 更多“当波距S>10mm,并不呈周期性变化的属于()。”相关的问题
更多“当波距S>10mm,并不呈周期性变化的属于()。”相关的问题
第2题
研究下列化学振荡:H2O2与KIO3在稀H2SO4溶液中的催化反应,在一定条件下,释放出O2的速率以及I2的浓
度会随时间呈周期性的变化。其主要反应(离子方程式)为 (1)IO3+H2O2→I2+O2 (2)H2O2+I2→IO3-+H2O 当系统中有过量H2O2参与并含有淀粉指示剂时,这种振荡能显示出蓝色和无色的周期性变化。请配平酸性溶液中进行的化学振荡(离子)反应(1)和(2),并说明其中H2O2所起的作用。 分析化学振荡是一种重要的自组织现象。当本题振荡反应停止后,若再加H2O2,又会继续前面的周期性变化。在(1)中H2O2作还原剂被氧化为O2,在(2)中H2O2作氧化剂将I2氧化为无色的IO3-而自身被还原为H2O。
点击查看答案
第3题
研究下列化学振荡:H2O2与KIO3在稀H2SO4溶液中的催化反应,在一定条件下,释放出O2的速率以及12的浓度会随时间
研究下列化学振荡:H2O2与KIO3在稀H2SO4溶液中的催化反应,在一定条件下,释放出O2的速率以及12的浓度会随时间呈周期性的变化。其主要反应(离子方程式)为(1)

当系统中有过量的H2O2参与并含有淀粉指示剂时,这种振荡能显示出蓝色和无色的周期性变化。请配平酸性溶液中进行的化学振荡(离子)反应(1)和(2),并说明其中H2O2所起的作用。
第8题
正常心电图QRS综合波形态哪些正确: ()
A.V1、V2 呈rS型,R/S< 1
B.V3导联呈RS型,R/S = 1
C.V5 导联呈qRs、Qr、Rs 或R型
D.从V1至V5 R波逐渐增大,S波逐渐减小
E.aVR导联的主波方向向上
第9题
左心房肥大的心电图诊断标准: ()
A.P波增宽≥ 0.12s
B.P波呈双峰,峰距≥ 0.04s
C.Ptfv1 ≤- 0.04mm.s 或负值增大
D.P波振幅在肢体导联≥ 0.25mV
E.P波振幅在胸导联≥ 0.20mV
第10题
波源的振动方程为(cm),它所形成的波以2m/s的速度沿x负方向传播。则沿x轴正方向上距波源6m处一点的振动方程为
波源的振动方程为y=6cosπ /5· t(cm),它所形成的波以2m/s的速度沿x负方向传播。则沿x轴正方向上距波源6m处一点的振动方程为______。
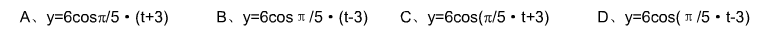
第11题
《普修规》护轨与基本轨头部间净距:在有砟桥上,其净距为()mm,允许误差为正10负5mm,当桥上设有调节器时,允许误差为正负10mm。
A.220
B.350
C.500
D.550


 如果结果不匹配,请
如果结果不匹配,请 

















