 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
Pb2+、Bi2+、Cu2+、Cd2+属于同一组离子,在一定的条件下都能与S2-生成硫化物沉淀,在氨性溶液中,()能与氨水生成络合离子而与其他离子分离。
A.Cu2+
B.Pb2+
C.Bi2+
D.Cd2+
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.Cu2+
B.Pb2+
C.Bi2+
D.Cd2+
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“Pb2+、Bi2+、Cu2+、Cd2+属于同一组离子,在一定…”相关的问题
更多“Pb2+、Bi2+、Cu2+、Cd2+属于同一组离子,在一定…”相关的问题
A.KspΘ(MnS)<KspΘ(CuS)<KspΘ(CdS)<KspΘ(PbS)
B.KspΘ(MnS)<KspΘ(CuS)、KspΘ(CdS)、KspΘ(PbS)
C.KspΘ(MnS)>KspΘ(CuS)、KspΘ(CdS)、KspΘ(PbS)
D.KspΘ(MnS)>KspΘ(CuS)>KspΘ(CdS)>KspΘ(PbS)
A.#图片0$#
B.#图片1$#
C.#图片2$#
D.#图片3$#
A.滴定Ni2+,Mn2+等不干扰
B.滴定Cu2+时, Zn2+,Cd2+等不干扰
C.可在大量Ca2+存在下滴下Mg2+
D.可在大量Mg2+存在下流走Ca2-
mol·L-1Pb2+to reach an endpoint using xylenol orange. Find the concentration of Cu2+in the unknown.
已知

Cd|Cd2+(0.10mol·L-1)||Sn4+(0.10mol·L-1),Sn2+(0.0010mol·L-1)|Pt在298K时的电动势ε,并写出电池反应,标明正、负极。
离子Ag+、Br-、Cd2+、Sc3+、Se2-、Sr2+、Ti2+、Zn2+中与Kr为等电子体的是
(A) Cd2+、Sr2+、Zn2+(B) Br-、Se2-、Sr2+
(C) Cd2+、Sc3+、Sr2+(D) Ag+、Br-、Sc3+
浓差电池
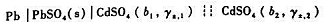
|PbSO4(s)|Pb,其中b1=0.2mol·kg-1.ya.1=0.1;b2=0.02mol·kg-1.Ya.z=0.32.已知在两液体接界处Cd2+的迁移数的平均值为t(Cd2+)=0.37.
(1)写出电池反应:
(2)计算25℃时液体接界电势E(液接)及电池电动势E.
当试液中Bi3+、Pb2+的浓度各为0.01mol/L,欲用EDTA标准溶液连续滴定Bi3+、Pb2+时,试选择滴定的酸度条件。