 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
可逆反应为了提高CO的平衡转化率,可以采用的措施是()。A、增大总压力 B、升高温度 C、增大H2⌘
A.增大总压力
B.升高温度
C.增大H2O(g)的分压
D.加入催化剂
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.增大总压力
B.升高温度
C.增大H2O(g)的分压
D.加入催化剂
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“可逆反应为了提高CO的平衡转化率,可以采用的措施是()。A、…”相关的问题
更多“可逆反应为了提高CO的平衡转化率,可以采用的措施是()。A、…”相关的问题
 CO2(g)+H2(g)ΔH<0,要提高CO的转化率可以用的方法是( )。
CO2(g)+H2(g)ΔH<0,要提高CO的转化率可以用的方法是( )。A.增大系统总压
B.减小系统总压
C.增加H2O的量
D.增加CO的量
dP(mm) | 3.175 | 6.35 | 9.525 |
R【mol/(s·g(cat))】 | 4.85×10-4 | 4.01×10-4 | 3.54×10-4 |
为了减少固定床反应器的压降,克服粒内阻力,希望采用的最大颗粒直径为多少?
已知
(忽略热效应影响,反应能保证在50℃进行)
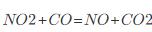 已经达到平衡状态的是( )
已经达到平衡状态的是( )A.CO和NO2不再反应
B.CO、NO2、CO2和NO的浓度相等
C.CO、NO2、CO2和NO的浓度比为1:1:1:1
D.CO、NO2、CO2和NO的浓度保持不变
反应 在某温度T时,Kc=9.0。若CO和H2O的起始浓度皆为0.02mol·L-1,计算平衡时各物质的浓度和CO的平衡转化率。
在某温度T时,Kc=9.0。若CO和H2O的起始浓度皆为0.02mol·L-1,计算平衡时各物质的浓度和CO的平衡转化率。
A. 化学平衡状态是正逆反应都停止的状态
B. 对于可逆反应C(s)+ H20(g) = CO(g) + H2(g),在一定温度下达到平衡,ρ(H20)=ρ(CO)=ρ(H2) ,即反应物与生成物压力相等
C. 反应N2(g) +02(g) =2NO(g)和2N2(g) +202(g) =4NO(g)虽代表同一反应,但是它们的标准平衡常数不相等
D. 多步反应的总标准平衡常数为各步反应标准平衡常数之和
已知反应 在1173K达到平衡时,测得平衡常数Kc=1.00。若在100L密闭容器中加入CO和水蒸气各200mol,试求算在该温度下的CO转化率。
在1173K达到平衡时,测得平衡常数Kc=1.00。若在100L密闭容器中加入CO和水蒸气各200mol,试求算在该温度下的CO转化率。
A.C6H5C2H5(g) = C6H5C2H3(g) + H2(g)
B.CO(g) + H2O(g) = CO2(g) + H2(g)
C.3/2 H2(g) + 1/2 N2(g) = NH3(g)
D.CH3COOH(l) + C2H5OH(l) = H2O(l) + C2H5COOH3(l)
反应C(s)+H2O(g)=CO(g)+H2(g),为提高C(s)的转化率,可采取()措施。
A.增加C(s)的用量
B.增加H2O(g)的浓度
C.按1:1增加,C(s)和H2O(g)的用量
D.以上三种方法都可以
若改变影响化学平衡的一个条件,使平衡向正反应方向移动,一定能提高某种反应物的转化率。()
化剂的活性下降。为了保持所要求的转化率,将原料进口温度提高至470℃,出口物料温度相应升至448℃;若反应的活化能为83.7kJ/mol,试估计催化剂活性下降的百分数。