题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
298.15K,101.325kPa下,1mol过饱和水蒸气变为同温同压下的液态水.求此过程的ΔS及ΔG,并判断此过程能否自动进行.已知298.15K时水的饱和蒸气压为3.166kPa,质量蒸发焓为2217J·g-1.
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“298.15K,101.325kPa下,1mol过饱和水蒸气…”相关的问题
更多“298.15K,101.325kPa下,1mol过饱和水蒸气…”相关的问题
已知水在101.325kPa,100℃下的摩尔蒸发焓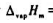 =40.668kJ·mol-1,现有2mol水蒸气在100℃,101.325kPa条件下凝结为液体水,此过程的ΔH=()kJ,Q=()kJ,W=()kJ,ΔU=()kJ.
=40.668kJ·mol-1,现有2mol水蒸气在100℃,101.325kPa条件下凝结为液体水,此过程的ΔH=()kJ,Q=()kJ,W=()kJ,ΔU=()kJ.
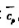 .已知水在100℃,101.325kPa下的摩尔蒸发焓
.已知水在100℃,101.325kPa下的摩尔蒸发焓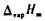 =40.668kJ·mol-1,水的平均摩尔定压热容
=40.668kJ·mol-1,水的平均摩尔定压热容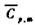 =75·32J·mol-1·K-1.
=75·32J·mol-1·K-1.
根据298.15K,pΘ时物质的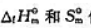 值,(1)求下列反应CO2(g)+2NH3(g)=CO(NH2)2(s)+H2O(l)的
值,(1)求下列反应CO2(g)+2NH3(g)=CO(NH2)2(s)+H2O(l)的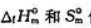 ;(2)计算上述反应在298.15K及pΘ下的ΔrGΘm值,.并判断由CO2(g)和NH3(g)反应生成尿素是否为自发过程.
;(2)计算上述反应在298.15K及pΘ下的ΔrGΘm值,.并判断由CO2(g)和NH3(g)反应生成尿素是否为自发过程.
已知水(H2O,I)在100℃的饱和蒸气压p=101.325kPa,在此温度.压力下水的摩尔蒸发焓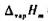 =40.668kJ·mol-1.求在100℃,101.325kPa下使1kg水蒸气全部凝结成液体水时的Q,W,ΔU和ΔH.设水蒸气适用理想气体状态方程.
=40.668kJ·mol-1.求在100℃,101.325kPa下使1kg水蒸气全部凝结成液体水时的Q,W,ΔU和ΔH.设水蒸气适用理想气体状态方程.
在总压101.325kPa下,正庚烷一正辛烷的气液平衡数据如下。
| 温度 /℃ | 液相中正庚烷的 摩尔分数(x) | 气相中正庚烷的 摩尔分数(y) | 温度 /℃ | 液相中正庚烷的 摩尔分数(x) | 气相中正庚烷的 摩尔分数(y) |
| 98.4 105 110 | 1.0 0.656 0.487 | 1.0 0.81 0.673 | 115 120 125.6 | 0.311 0.157 0 | 0.491 0.280 0 |
试求: