题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
实验测定气一固催化反应速率与温度关系如下: T(℃) 100 200 反应速率【mo
实验测定气一固催化反应速率与温度关系如下:
T(℃) | 100 | 200 |
反应速率【mol/(kg·min)】 | 50 | 68 |
请判断内扩散对过程是否有影响,为什么。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
实验测定气一固催化反应速率与温度关系如下:
T(℃) | 100 | 200 |
反应速率【mol/(kg·min)】 | 50 | 68 |
请判断内扩散对过程是否有影响,为什么。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“实验测定气一固催化反应速率与温度关系如下: T(℃) 100…”相关的问题
更多“实验测定气一固催化反应速率与温度关系如下: T(℃) 100…”相关的问题
(1)有一同学在取样的时候,没有严格控制进样量,是否正确,为什么?外标法的优点是什么?
(2)有一同学想改用高效液相色谱-紫外检测器来进行这两种残留溶剂的定量检测,是否可行?为什么?
(3)照《中国药典》残留溶剂测定法测定。采用6%氰苯基聚硅氧烷和94%的二甲基硅氧烷为固定相的毛细管色谱柱;程序升温,初始温度为40℃,维持4分钟,再以每分钟30℃的升温速率升至200℃,维持6分钟;检测器为火焰离子化检测器。
试说明柱温对气相色谱分离有什么影响?程序升温相对恒定柱温有什么优势?
(4)有一同学想对实验条件进行优化,作了如下尝试,试讨论下列每一个条件单独改变时,分析物的保留时间和色谱峰形会发生怎样的变化(假设在任何条件下,两种分析物均能完全分离)。
(A)色谱柱柱长减小1/3;
(B)载气流速从1.0ml/min改变到1.2ml/min;
(C)柱温以每分钟20℃的升温速率升至200℃。
为测定化学反应:

的反应级数、得到如下初始反应速率与反应物初始浓度关系的实验数据。
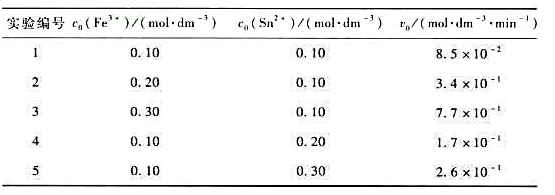
试计算反应对于Fe3+和Sn3+的反应级数;写出反应的速率方程并求出速率常数。
H2O2与I在酸性溶液中发生下列反应:

在某一温度下,测定的实验数据如下:

(1)确定该反应的反应级数,并写出速率方程;
(2)计算该反应的速率系数;
(3)当c(H2O2)=5.0×10-2mol·L-1,c(H+)=1.0×10-²mol·L-1,
c(I-)=2.0×10-2mol·L-1时,反应速率为多少?
一定温度下,对反应2A====B+D,实验测定了如下数据:
cA/(mol·L-1) 0.40 0.20
速率/(mol·L-1·min-1) 0.02 0.01
则该反应的速率方程为r=______,速率常数k=______。
现要实验测定一传热面积为4m2的套管式换热器的总传热系数K值。实验情况如下:所用热水走管内,其流量为2000kg/h,进口温度为90℃,出口温度为40℃;所用冷水走管外,测得进口温度为20℃,出口温度为40℃,两流体做逆流流动。试求其总传热系数K。
某工厂进行反应A→P实验,从相同浓度cA0=10mol/L开始,测得数据如下:
序号 | T(℃) | x(%) | t(h) |
1 | 120 | 99 | 5.5 |
2 | 20 | 90 | 576 |
3 | 120 | 90 | 0.5 |
试求反应级数,并求反应速率常数与温度的关系式。
N2O(g)的 热分解反应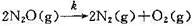 ,从实验测出不同温度时,各个起始压力po与半衰期t1/2的值如下:
,从实验测出不同温度时,各个起始压力po与半衰期t1/2的值如下:
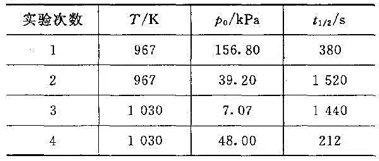
试求:(1)反应级数和不同温度下的速率常数; (2)反应的实验活化能E,值;(3)若1 030 K时,N2O(g)的初始压力为54.00kPa,当压力达到64.00kPa时,所需的时间。
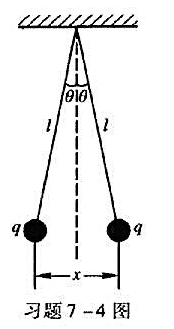
为了验证库仑定律点电荷之间的作用力与距离的关系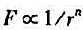 中n=2,有人构思了如下的实验:两相同的金属小球用两根相同长的悬线吊在O点上,如图所示,如果它们均带电荷q,则可测定它们之间的排斥距离为x1;如果它们均带电荷q/2,则可测定它们之间的排斥距离为x2,图中θ角很小。请由此导出库仑定律中的幂指数n与x1、x2的关系式。
中n=2,有人构思了如下的实验:两相同的金属小球用两根相同长的悬线吊在O点上,如图所示,如果它们均带电荷q,则可测定它们之间的排斥距离为x1;如果它们均带电荷q/2,则可测定它们之间的排斥距离为x2,图中θ角很小。请由此导出库仑定律中的幂指数n与x1、x2的关系式。