 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
17. 25℃时,上述反应在80%乙醇水溶液中进行,t-C5H11I的初始浓度约为0.02mol·kg-1,各不同时刻的导电数据如表1
17. 25℃时,上述反应在80%乙醇水溶液中进行,t-C5H11I的初始浓度约为0.02mol·kg-1,各不同时刻的导电数据如表11-12所示。求速率常数k。
表11-12
|
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
17. 25℃时,上述反应在80%乙醇水溶液中进行,t-C5H11I的初始浓度约为0.02mol·kg-1,各不同时刻的导电数据如表11-12所示。求速率常数k。
表11-12
|
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“17. 25℃时,上述反应在80%乙醇水溶液中进行,t-C5…”相关的问题
更多“17. 25℃时,上述反应在80%乙醇水溶液中进行,t-C5…”相关的问题
末期反应时间与转化率
蔗糖在稀水溶液中水解生成葡萄糖和果糖的反应为
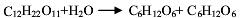

当水大大过量时,反应遵循一级反应动力学,即(-rA)=kcA,在催化剂HCl浓度为0.01mol/L,反应温度为48℃时,反应速率常数为k=0.0193min-1。当蔗糖的浓度为0.1mol/L和0.5mol/L时计算:
(1)反应20min后,上述两种初始浓度下反应液中蔗糖、葡萄糖和果糖的浓度分别为多少?
(2)试计算两种初始浓度的溶液中蔗糖的转化率各为多少?
(3)若蔗糖浓度降到0.01min/L时,两种初始浓度条件下所需反应时间各为多少?
反应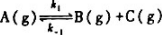 中,k1和k-1,在25℃时分别为0.2s-1和.3.9477x10-3MPa-1.s-1.在35℃时二者皆增为2倍.试求:
中,k1和k-1,在25℃时分别为0.2s-1和.3.9477x10-3MPa-1.s-1.在35℃时二者皆增为2倍.试求:
(1)25C时的反应平衡常数Kθ;
(2)正、逆反应的活化能及25℃时的反应热Qm;
(3)若上述反应在25℃的恒容条件下进行,且A的起始压力为100kPa,若要使总压达到152kPa,问需要反应多长时间?
反应 在某温度T时,Kc=9.0。若CO和H2O的起始浓度皆为0.02mol·L-1,计算平衡时各物质的浓度和CO的平衡转化率。
在某温度T时,Kc=9.0。若CO和H2O的起始浓度皆为0.02mol·L-1,计算平衡时各物质的浓度和CO的平衡转化率。
A.150
B.356
C.25
D.5.94
在25℃,CO2气体压力等于1标准大气压时,CO2饱和水溶液中CO2的浓度约为0.034 mol.dm-3,计算溶液的pH和[CO32-]。通常把溶入的CO2都当成H2CO3,利用如下平衡式计算: H2CO3+H2O
 HCO3-+H3O+ Ka1=4.5×10-7
HCO3-+H3O+ Ka1=4.5×10-7
在一定的反应温度下A发生下述平行反应:
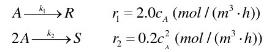
其中R是主产物,S是副产物。反应原料为纯的反应物A,其初始浓度为10kmol/m3。在反应器出口A的转化率为80%。请比较当上述反应在连续搅拌釜和管式连续流动反应器中进行时,A转化为R的选择率、R的收率以及反应物的停留时间有什么不同。在反应过程中体积的变化可以忽略不计。
t/s | 0 20 30 40 50 60 70 80 |
c(t)/g·m-3 | 0 3 5 5 4 2 1 0 |
物料流量qV=0.1m3·s-1。若该反应在CSTR中进行,在同样


双分子可逆反应的计算
在100℃下进行酯化反应,采用盐酸作催化剂,反应式为
CH3COOH+C2H5OH=====CH3COOC2H5+H2O
(A) (B) (P) (S)
反应动力学方程为
(-rA)=k1cAcB-k2cPcS
其中:k1=4.76×10-4m3/(kmol·min)
k2=1.63×10-4m3/(kmol·min)
若反应在一间歇反应器中进行,投料量为0.3785m3水溶液,其中含有90.8kg乙酸和181.6kg乙醇。反应过程物系的密度为1043kg/m3,计算反应120min时,乙酸的转化率为多少?其平衡转化率为多少?
男性,30岁。高热待查,体温39.8℃,遵医嘱行乙醇拭浴降温。用的乙醇浓度为A、10%~20%
B、25%~35%
C、40%~50%
D、60%~70%
E、70%~80%
错误的操作方法是A、头部先放冰袋,足部放热水袋
B、以拍拭方式进行,不用摩擦方式
C、腋窝、腹股沟适当延长拍拭时间
D、禁忌拍拭胸前区、腹部和足底等部位
E、病人发生寒战、面色苍白时应减慢速度
乙醇拭浴后观察降温效果,为病人测体温应在拭浴后A、10min
B、15min
C、20min
D、30min
E、60min
体温降至何种程度应取下头部冰袋A、37.5℃以下
B、38℃以下
C、38.5℃以下
D、39℃以下
E、39.5℃以下
A.700ml
B.797ml
C.638ml
D.730ml
E.640ml