 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在氨水中加入NH4Cl后,NH3的α和pH的变化分别是( )。
A.α和pH都增大
B.α减小,pH增大
C.α增大,pH变小
D.α和pH都减小
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.α和pH都增大
B.α减小,pH增大
C.α增大,pH变小
D.α和pH都减小
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在氨水中加入NH4Cl后,NH3的α和pH的变化分别是()。…”相关的问题
更多“在氨水中加入NH4Cl后,NH3的α和pH的变化分别是()。…”相关的问题
)2沉淀生成.若此NH3·NH4Cl混合溶液中NH3的浓度0.10mol·L-1,则此混合溶液中NH4Cl的浓度至少为多少?
A.NaOH:电解槽的阴极产生的是H2,NaOH在阳极附近产生
B.H2SO4:在高温高压下转化SO2,提高转化率和反应速率
C.NH3:氮氢循环操作,提高NH3平衡浓度
D.Na2CO3:分离NaHCO3后的母液中加入食盐,促进NH4Cl结晶
在1mL 0.04mol·L-1AgN03溶液中,加入1mL 2.00mol·L-1氨水,计算平衡后溶液中的Ag+浓度。已知Kf([Ag(NH3)2]+)=1.6×107。
A.KAl(SO4)2溶液加热
B.Na2CO3溶液加热
C.氨水中加入少量NH4Cl固体
D.NH4NO3溶液中加入少量NaNO3固体
已知氨水的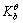 =1.8x10-5,现有1.0dm30.10mol·dm-3氨水,试求:
=1.8x10-5,现有1.0dm30.10mol·dm-3氨水,试求:
(1)氨水的c(H+);
(2)加入10.7gNH4Cl后,溶液的c(H+)(假设加入NH4Cl后溶液体积的变化可以忽略不计);
(3)加入NH4Cl后,氨水的解离度缩小的倍数。
在浓度为0.20mol·L-1、体积为100mL的MgCl2溶液中,加入等体积等浓度的氨水,
(1)问有无沉淀生成?
(2)为阻止沉淀生成,需要加入多少克固体NH4Cl?
欲配pH=10.0的缓冲溶液,计算应在300mL0.5mol·L-1NH3·H2O溶液中加入NH4Cl的质量。
A.所有铵盐受热均可以分解,产物均有NH3
B.所有铵盐都易溶于水,所有铵盐中的N均呈-3价
C.NH4Cl溶液中加入NaOH浓溶液共热时反应的离子方程式为NH4++OH-=(加热)NH3↑+H2O
D.NH4Cl和NaCl的固体混合物可用升华法分离