 更多“设HAc溶液的分析浓度为c,则下列平衡浓度关系正确的是()”相关的问题
更多“设HAc溶液的分析浓度为c,则下列平衡浓度关系正确的是()”相关的问题
在298 K时,醋酸HAc的解离平衡常数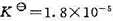 ,试计算在下列不同情况下醋酸在浓度为1.0mol·kg-1时的解离度。(1)设溶液是理想的,活度因子均为1;(2)用Debye-Huckel极限公式计算出γ±的值,然后再计算解离度。设未解离的HAc的活度因子为1.
,试计算在下列不同情况下醋酸在浓度为1.0mol·kg-1时的解离度。(1)设溶液是理想的,活度因子均为1;(2)用Debye-Huckel极限公式计算出γ±的值,然后再计算解离度。设未解离的HAc的活度因子为1.
A.c(HAc)=[H⁺][Ac⁻]
B.c(HAc)=c(NaOH)
C.[H⁻]=[Ac⁻]+[OH⁻]
D.[H⁻]+[HAc]=[OH⁻]
A.NaHCO3中含有氢,故其水溶液呈酸性
B.浓HAc(17mol/L)的酸度大于17mol/L H2SO4水溶液的酸度
C.浓度(单位:mol/L)相等的一元酸和一元碱反应后,其溶液呈中性
D.弱酸溶液愈稀,其电离度愈大,因而酸度亦愈大
E.当[H+]大于[OH-]时,溶液呈酸性
A.NaHCO3中含有氧,故其水溶液呈酸性
B.浓HAc(17mol/L)的酸度大于1mol/L H2SO4水溶液的酸度
C.浓度(单位:mol/L)相等的一元酸和一元碱反应后,其溶液呈中性
D.弱酸溶液愈稀,其电离度愈大,因而酸度亦愈大
E.当c(H+)大于c(OH-)时,溶液呈酸性
某溶液中含有HAc、NaAc和Na2C2O4,其浓度分别为0.80mol/L、0.29mol/L、1.0×10-4mol/L。计算此溶液中 C2O42-的平衡浓度。
A.HAc-HCI混合溶液
B.NH4Ac溶液
C.HAc-NaAc混合溶液
D.pH=5.00的溶液
已知Cu(OH)2的
下列四种物质的量浓度相同的稀溶液,渗透压符合下面关系的是()。
A.HAc>NaCl>C6H12O6>CaCl2
B.C6H12O6>HAc>NaCl>CaCl2
C.CaCl2>HAc>C6H12O6>NaCl
D.CaCl2>NaCl>HAc>C6H12O6

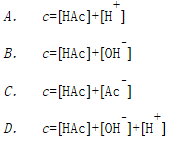

 如果结果不匹配,请
如果结果不匹配,请 

















