 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
根据价层电子对互斥模型,判断下列分子或者离子的空间构型不是三角锥形的是()
A.PCl3
B.H3O+
C.HCHO
D.PH3
 答案
答案
C、HCHO
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.PCl3
B.H3O+
C.HCHO
D.PH3
 答案
答案
C、HCHO
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“根据价层电子对互斥模型,判断下列分子或者离子的空间构型不是三…”相关的问题
更多“根据价层电子对互斥模型,判断下列分子或者离子的空间构型不是三…”相关的问题
试根据价层电子对互斥理论推出下列情况下ABn型分子的几何构型:
(1)中心原子A的价层电子对数为6,配体B的个数n=4;
(2)中心原子A的价层电子对数为5,配体B的个数n=2。
并利用得出的结论判断下列分子或离子的几何构型:
(3)I3-;(4)XeF2;(5)XeF4;(6)ICl4-。
简要回答下列问题:
(1)电解NaCl熔盐制取金属Na的过程中,为什么要加入CaCl2?由此带来的负面影响是什么?
(2)为什么金属Mg与冷水反应极慢,却可以迅速与热水或NH4Cl水溶液发生反应?
(3)什么是离子势φ?为什么φ的大小可以影响一些氧化物的水化物的解离方式?
(4)为什么加热MgCl2·6H2O时得不到无水盐?
(5)为降低煤炭燃烧时排向大气的SO2量,可以把CaO或CaCO3掺到含硫的煤炭中。试说明这种做法的化学原理,写出相关的化学反应方程式。
(6)Li+和Mg2+半径十分接近,试分析它们的碳酸盐分解温度的高低。
(7)锂的第一电离能比钠大,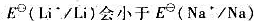 ?既然
?既然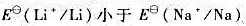 ,为什么锂与水的反应却不如钠剧烈?
,为什么锂与水的反应却不如钠剧烈?
(8)试说明锂的哪些性质与镁相似而有别于钠、钾。
(9)试说明铍的哪些性质与铝相似而有别于镁、钙。
(10)试用价层电子对互斥理论和杂化轨道理论,讨论XeF6分子的几何构型和中心原子的轨道杂化方式。
A.设计模型应严格根据建模要求建立模型,并在iTWo系统中进行初步的模型检测
B.只可以根据业主招标所用的工程量清单
C.在投标阶段可以根据地方定额或企业定额进行清单的组价工作,在施工阶段可以根据企业消耗定额来编制项目施工成本清单,变更清单可以根据合同要求进行编制
D.根据施工成本清单或目标清单进行清单的分解,生成分包任务进行招标、评标、定标管理工作
根据下列分子偶极矩数据,判断分子的极性和几何构型。
SiCl4(μ=0),CH3Cl(μ=6.38×10-30C·m),SO3(μ=0),BCl3(μ=0),PCl3(μ=2.6×10-30C·m)。