 更多“系统经绝热过程由始态到末态,若经历的过程是不可逆的,熵将()…”相关的问题
更多“系统经绝热过程由始态到末态,若经历的过程是不可逆的,熵将()…”相关的问题
第1题
始态为25°C,200kPa的5mol某理想气体,经途径a,b两不同途径到达相同的末态。途经a先经绝热膨胀到-28.47C,100kPa,步骤的功Wa=-5.57kJ;再恒容加热到压力200kPa的末态,步骤的热Qa=25.42k.途径b为恒压加热过程。求途径b的Wb及Qb.
第3题
1mol理想气体在T=300K下,从始态100kPa经历下列过程达到各自的平衡态。求各过程的Q,ΔS,ΔSiso (1)可逆膨胀至末态压力50kPa; (2)反抗恒定外压50kPa不可逆膨胀至平衡态: (3)向真空自由膨胀至原体积的2倍。
1mol理想气体在T=300K下,从始态100kPa经历下列过程达到各自的平衡态。求各过程的Q,ΔS,ΔSiso (1)可逆膨胀至末态压力50kPa; (2)反抗恒定外压50kPa不可逆膨胀至平衡态: (3)向真空自由膨胀至原体积的2倍。
点击查看答案
第4题
某封闭系统,若系统初始U为100kJ/mol,将系统降温,内能变为40kJ/mol,再升温,内能为200kJ/mol,则系统由始态到终态内能的变化量是多少()。
A.100kJ/mol
B.160kJ/mol
C.220kJ/mol
D.200kJ/mol
第5题
2mol某双原子理想气体的Sθm(298K)=205.1J.mol-1.K-1.从298K,100kPa的始态.沿pT=常数的途径可逆压缩到200kPa的末态,求该过程的Q,W,ΔU,ΔH,ΔS和ΔG.
2mol某双原子理想气体的Sθm(298K)=205.1J.mol-1.K-1.从298K,100kPa的始态.沿pT=常数的途径可逆压缩到200kPa的末态,求该过程的Q,W,ΔU,ΔH,ΔS和ΔG.
点击查看答案
第6题
已知氮(N2,g)的摩尔定压热容与温度的两数关系为将始态为300K,100kPa下的1molN2(g)置于
已知氮(N2,g)的摩尔定压热容与温度的两数关系为将始态为300K,100kPa下的1molN2(g)置于
点击查看答案
已知氮(N2,g)的摩尔定压热容与温度的两数关系为
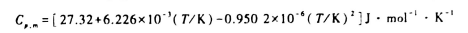
将始态为300K,100kPa下的1molN2(g)置于1000K的热源中,求系统分别经(1)恒压过程;(2)恒容过程达到平衡态时的Q,ΔS及ΔSm.
第7题
化学反应如下: (1)利用附录中各物质的数据,求上述反应在25°C时的 (2)利用附录中各物质的
化学反应如下: (1)利用附录中各物质的数据,求上述反应在25°C时的 (2)利用附录中各物质的
点击查看答案
化学反应如下:
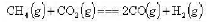
(1)利用附录中各物质的数据,求上述反应在25°C时的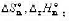
(2)利用附录中各物质的数据,计算上述反应在25°C时的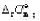
(3)25°C若始态CH4(g)和H2(g)的分压均为150kPa,末态CO(g)和H2(g)的分压均为50kPa,求反应的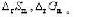
第8题
体系从同一初态到同一终态,经历二个不同过程,一为可逆过程,一为不可逆过程,此二过程环境熵变存在()。
A.(ΔS环)可逆<(ΔS环)不可逆
B.(ΔS环)可逆>(ΔS环)不可逆
C.(ΔS环)可逆=(ΔS环)不可逆
D.(ΔS环)可逆=0
第10题
如图8.2所示,体系由图中A态经ABC过程到达C态,吸收的热量为350J,同时对外做功126J。 (1)如果沿A
如图8.2所示,体系由图中A态经ABC过程到达C态,吸收的热量为350J,同时对外做功126J。 (1)如果沿A
点击查看答案
如图8.2所示,体系由图中A态经ABC过程到达C态,吸收的热量为350J,同时对外做功126J。
(1)如果沿ADC进行,系统对外做功为42J,则系统吸收了多少热量?
(2)如果系统由C出发沿CA曲线返回A,外界对系统做功为84J,则系统吸热多少?



 如果结果不匹配,请
如果结果不匹配,请 

















