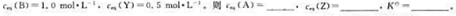题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
298.15K时,
298.15K时,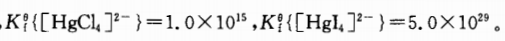 。则下列反应:
。则下列反应: 在298.15K时的标准平衡常数为()。
在298.15K时的标准平衡常数为()。
A.5.0×1044
B.2.0×10-15
C.5.0×1014
D.2.0×10-45
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
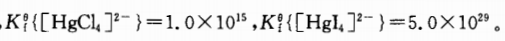 。则下列反应:
。则下列反应: 在298.15K时的标准平衡常数为()。
在298.15K时的标准平衡常数为()。A.5.0×1044
B.2.0×10-15
C.5.0×1014
D.2.0×10-45
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“298.15K时,。则下列反应:在298.15K时的标准平衡…”相关的问题
更多“298.15K时,。则下列反应:在298.15K时的标准平衡…”相关的问题
 分别为
分别为 (1)和
(1)和 (2): (1)MnO2(s)====MnO(s)+
(2): (1)MnO2(s)====MnO(s)+ O2(g) (2)MnO2(S)+Mn(s)====2MnO(s) 则298 K时,MnO2(S)的
O2(g) (2)MnO2(S)+Mn(s)====2MnO(s) 则298 K时,MnO2(S)的 等于( )。
等于( )。A.
B.
C.
D.
已知四氧化二氮的分解反应如下:

在298.15K时,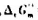 =4.75kJ·mol-1.试判断在此温度及下列条件下,反应进行的方向.
=4.75kJ·mol-1.试判断在此温度及下列条件下,反应进行的方向.
已知下列反应在298.15K的平衡常数:
(1)SnO2(s)+2H2(g) 2H2O(g)+Sn(s)
2H2O(g)+Sn(s)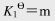
(2)H2O(g)+CO(g) H2(g)+CO2(g);
H2(g)+CO2(g);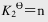
计算反应2CO(g)+SnO2(s) Sn(s)+2CO2(g)在298.15K时的平衡常数KΘ3。
Sn(s)+2CO2(g)在298.15K时的平衡常数KΘ3。
A.△rHөm<0,△rSөm>0
B.△rHөm>0,△rSөm>0
C.△rSөm<0,△rHөm>0
D.△rGөm(298.15K)<0
已知四氧化二氮的分解反应为N2O4(g)===2NO2(g)。在298.15K时,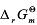 =4.75kJ·mol-1。试判断在此温度及下列条件下,反应进行的方向。
=4.75kJ·mol-1。试判断在此温度及下列条件下,反应进行的方向。
(1)N2O4(g,100kPa),NO2(g,100kPa);
(2)N2O4(g,1000kPa),NO2(g,100kPa);
(3)N2O4(g,300kPa),NO2(g,200kPa)。
已知298.15K时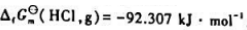 化学反应
化学反应
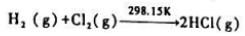
在催化剂的作用下反应速率大大加快时,反应的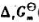 (298.15K)=().
(298.15K)=().
在1.5mol·L-1A溶液中加入一定量B,在298.15K时发生反应: 当反应达到平衡时.
当反应达到平衡时.