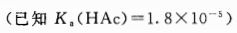题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
25℃时,pH(HAc)=4.74。将20mL0.10mol·L-1HAc溶液与10ml.0.10mol·L-1NaOH溶液混合.计算所得混合溶液的pH。
25℃时,pH(HAc)=4.74。将20mL0.10mol·L-1HAc溶液与10ml.0.10mol·L-1NaOH溶液混合.计算所得混合溶液的pH。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“25℃时,pH(HAc)=4.74。将20mL0.10mol…”相关的问题
更多“25℃时,pH(HAc)=4.74。将20mL0.10mol…”相关的问题
HAc 的 ρK.= 4.74 , 用它配制缓冲溶液的 pH 缓冲范围是() , NH3 的 ρKb= 4.76 ,其配制缓冲榕液的 pH 缓冲范围是()。
已知25℃时,Ka(HAc)=1.75×10-5。计算该温度下0.10mol·L-1HAc溶液中H+浓度及溶液的pH,并计算该浓度下HAc的解离度。
A.c(HCl)=0.1mol/L HCl溶液
B.c(NH3)=0.1mol/L NH3·H2O溶液
C.c(HAc)=0.1mol/L HAc溶液
D.c(HAc)=0.1mol/L HAc溶液+c(NaAc)=0.1mol/L NaAc溶液
A.1.76
B.4.75
C.5
D.2
25℃时




A.0.1mol/L HCl
B.1mol/L NH3·H2O
C.1mol/L HAc
D.1mol/L HAc+1mol/L NaAc
E.1mol/L NH3·H2O+1mol/L NH4Cl
A.8.77~9.70
B.7.77~9.70
C.6.77~9.70
D.7.77~10.70
0.35mol·L-1 HAc溶液与0.45mol·L-1NaAc 等体积混合,计算混合溶液的pH值。