 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
100kPa和100℃下,将一定体积的O2与2.0dm3H2爆炸反应,反应后气体的体积等于反应前H2
(1)爆炸反应后100C时H2的分压;
(2)反应前O2的体积;
(3)反应后85℃时气体的体积。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
(1)爆炸反应后100C时H2的分压;
(2)反应前O2的体积;
(3)反应后85℃时气体的体积。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“100kPa和100℃下,将一定体积的O2与2.0dm3H2…”相关的问题
更多“100kPa和100℃下,将一定体积的O2与2.0dm3H2…”相关的问题
在一定温度下,将1.0molNa2O2(g)放入一密闭容器中,发生下列可逆反应
 当达到化学平衡时,容器内有0.8molNO,气体总压为100kPa。则该可逆反应在此温度下的标准平衡常数为().
当达到化学平衡时,容器内有0.8molNO,气体总压为100kPa。则该可逆反应在此温度下的标准平衡常数为().
A、0.40
B、0.67
C、0.76
D、1.3
某种类型的煤含硫为3.0%(质量分数),问: (1)燃烧100g该种煤,将产生多少克二氧化硫? (2)在298K与100kPa下,将产生多少体积的SO2? (3)如采用1.00m3空气燃烧这部分煤,烟道气中SO2的浓度为多少?
如图所示,无摩擦、无质量、无体积的活塞1,2,3将反应器隔成甲、乙、丙3部分,分别进行反应
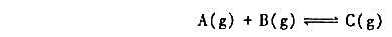
起始时物质的量已标在图中。某温度和100kPa下实现平衡时,各部分的体积分别为V甲,V乙,V丙。
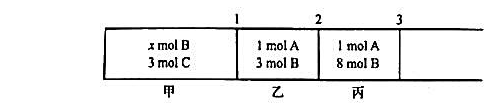
(1)这时若去掉活塞1,不会引起其他活塞移动,求算x值;
(2)去掉活塞2后再次达到平衡时,活塞3向哪个方向发生了移动?试通
过计算加以解释,可以假定反应的Kθ等于1。
用绝对压力为300kPa的饱和水蒸气将体积流量为80m3/h的苯胺从80℃加热到100℃。苯胺在平均温度下的密度为955kg/m3,比热容为2.31kJ/(kg·℃)。试求:
A.6x10-3;
B.6;
C.6000;
D.0.6
已知氮(N2,g)的摩尔定压热容与温度的两数关系为
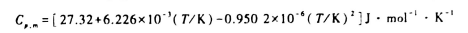
将始态为300K,100kPa下的1molN2(g)置于1000K的热源中,求系统分别经(1)恒压过程;(2)恒容过程达到平衡态时的Q,ΔS及ΔSm.
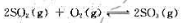
反应达到平衡时,测得混合物中有6.0molSO2(g)。试计算:
(1)该可逆反应在800K时的标准平衡常数和标准摩尔吉布斯自由能变;
(2)SO2在上述条件下的平衡转化率。
A.冰箱中使一定体积的空气保持在低于冰点的某一温度比使相同体积的冷冻食品保持该温度需要更多的能量
B.冰箱的门打开的次数越多,保持冰箱的正常温度所需的能量越多
C.当将未冷冻的食品放入冰箱中时,冰箱内的一定体积空气的平均温度会暂时升高
D.通常保持冰箱半空的人可以使用比该冰箱体积小一半的冰箱从而很大程度地削减能耗