 更多“说明I2易溶于CCl4,KI溶液的原因。”相关的问题
更多“说明I2易溶于CCl4,KI溶液的原因。”相关的问题
第2题
含有0.120g碘的KI溶液100mL,25℃时用25mLCCl4与之一起振摇,假设碘在CCl4和KI溶液之间的分配达到平衡后,在水
含有0.120g碘的KI溶液100mL,25℃时用25mLCCl4与之一起振摇,假设碘在CCl4和KI溶液之间的分配达到平衡后,在水中测得有0.00539g I2,试计算碘的分配系数。
第5题
称取含Kl之试样1.000g溶于水.加10mL0.05000mol·L-1KIO3溶液处理,反应后煮沸驱尽所
生成的I2,冷却后,加入过量KI溶液与剩余的KIO3反应.析出I2的需用21.14mL0.1008mol·L-1
点击查看答案
Na2S2O3溶液滴定.计算试样中KI的质量分数.
第6题
某同学设计完成了以下两个实验:①向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色(生成了HIO3)。②向盛有KBr溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成红棕色。继续向试管中滴加氯水,振荡,CCl4层的颜色没有变化。下列说法不正确的是()。
A.实验①生成HIO3时发生的反应为:I2+5Cl2+6H2O=2HIO3+10HCl
B.实验②中当CCl4层变成红棕色时可通过分液的方法获得Br2的CCl4溶液
C.由上述实验得出Cl2、Br2、I2的氧化性由强到弱的顺序是:Cl2>Br2>I2
D.由上述实验得出Cl2、HIO3、HBrO3氧化性由强到弱的顺序是:HBrO3>Cl2>HIO3
第7题
称取基准纯KIO30.8920g,溶于250ml量瓶中,稀释至刻度,吸取25.00ml该溶液于锥形瓶中,加酸及
过量的KI,析出的I2用Na2S2O3溶液滴定,消耗24.10ml,求Na2S2O3溶液的浓度(已知:MKIO3=214.00)。
点击查看答案
第8题
(1)25℃时将0.568g碘溶于50cm3CCl4中,所形成的溶液与500cm3水一起摇动,平衡后
(1)25℃时将0.568g碘溶于50cm3CCl4中,所形成的溶液与500cm3水一起摇动,平衡后
点击查看答案
测得水层中含有0.233mmol的碘.计算碘在两分中的分配系数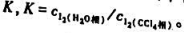 .设碘在两种溶剂中均以I2分子形式存在.
.设碘在两种溶剂中均以I2分子形式存在.
(2)若25℃I2在水中的浓度是1.33mmol.dm-3,求碘在CCl4中的浓度.
第9题
A的水合物为紫色品体。向A的水溶液中加入Na2CO3溶液有灰蓝色沉淀B生成。B溶于过量NaOH溶液得到绿色溶液C。向C
A的水合物为紫色品体。向A的水溶液中加入Na2CO3溶液有灰蓝色沉淀B生成。B溶于过量NaOH溶液得到绿色溶液C。向C中滴加H2O2得黄色溶液D。取少量D经醋酸酸化后加入BaCl2溶液则析出黄色沉淀E。将D用硫酸酸化后通入SO2得到绿色溶液F。将A的水溶液加入硫酸后加入KI溶液经鉴定有I2生成,同时放出无色气体G。G在空气中逐渐变为棕色。请给出各字母所代表的物质。
第10题
称取含有KI的试样0.5000g,溶于水后先用Cl2水氧化I-为,煮沸除去过量Cl2;再加入过量KI试剂,滴定I2时消耗了0.0
称取含有KI的试样0.5000g,溶于水后先用Cl2水氧化I-为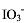 ,煮沸除去过量Cl2;再加入过量KI试剂,滴定I2时消耗了0.02082mol/L Na2S2O321.30mL。计算试样中KI的质量分数。
,煮沸除去过量Cl2;再加入过量KI试剂,滴定I2时消耗了0.02082mol/L Na2S2O321.30mL。计算试样中KI的质量分数。


 如果结果不匹配,请
如果结果不匹配,请 

















