 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知25℃时Ag2SO4饱和水溶液的电导率(Ag2SO4)=0.7598S.m-1,配制溶液所用
水的电导率k(H2O)=1.6x10-4S·m-1.离子极限摩尔电导率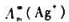 和
和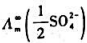 分别为
分别为
61.9x10-4s.m·mol-1和80.0x10-4s.m2mol-1.此温度下Ag2SO4的活度积Kap=().
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
水的电导率k(H2O)=1.6x10-4S·m-1.离子极限摩尔电导率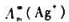 和
和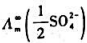 分别为
分别为
61.9x10-4s.m·mol-1和80.0x10-4s.m2mol-1.此温度下Ag2SO4的活度积Kap=().
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知25℃时Ag2SO4饱和水溶液的电导率(Ag2SO4)=…”相关的问题
更多“已知25℃时Ag2SO4饱和水溶液的电导率(Ag2SO4)=…”相关的问题
已知单效蒸发器每小时处理2tNaOH水溶液,溶液由10%(质量分数)浓缩到25%。加热蒸汽压强为400kPa(绝对压强),冷凝后在饱和温度下排出。假设蒸发器的热损失忽略不计,溶液的沸点为113℃,分别按20℃加料和沸点加料,求此两种情况下的加热蒸汽消耗量和单位蒸汽消耗量。
已知25℃时AgCl(s);水溶液中Ag+,CI-的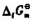 分别为-109.789kJ·mol-1,
分别为-109.789kJ·mol-1,
77.107kJ·mol-1和-131.228kJ·mol-1.求25℃下AgCl(s)在水溶液的标准溶度积Kθ及溶解度s.
当溶液中c(Ag+)=0.010mol·dm-3时,为了防止产生Ag2SO4沉淀,则溶液中

在一中央循环管式蒸发器内将浓度为10%(质量分数,下同)的NaOH水溶液浓缩到40%,二次蒸汽压强为40kPa,二次蒸汽的饱和温度为75℃。已知在操作压强下蒸发纯水时,其沸点为80℃。求溶液的沸点和由于溶液的静压强引起的温度升高的值。
10%及40%NaOH水溶液杜林线的斜率及截距如下:
| 质量分数/% | 斜率 | 截距 |
| 10 40 | 1.02 1.11 | 4.5 3.4 |
用镁离子选择电极测定溶液中的Mg2+,其电池的组成为
镁离子选择电极|Mg2+||饱和甘汞电极
在25℃时,c(Mg2+)=1.15×10-2mol·L-1时,该电池的电动势为0.275V,当用Mg2+试液代替已知溶液时,测得电动势为0.280V,计算试液的pMg。
用一单效蒸发器将2000kg/h的某水溶液由15%(质量分数)浓缩至25%(同上)。已知加热蒸汽压强为392kPa,溶液的平均沸点为113℃,进料温度为25℃,其水溶液的比热容为3.8kJ/(kg·℃),蒸发器的传热系数为1500W/(m2·℃),蒸发器的热损失为所需热量的3%。试求:
在一单效中央循环管式蒸发器内将浓度10%(质量分数,下同)的NaOH溶液浓缩到40%。二次蒸汽绝对压强为40kPa,相应的饱和温度为75℃。已知在操作压强下蒸发纯水时,液柱中部的沸点温度为80℃。试求溶液的沸点及由于溶液静压强引起的温度差损失。
10%及40%NaOH水溶液杜林线的斜率及截距如下:
| 斜率 | 截距 | |
10% 40% | 1.02 1.11 | 4.5 34 |
取剂用量为600kg,25℃时丙酮(A)-水(B)-三氯乙烷(S)系统的液-液相平衡数据列于下表(均为质量分数)。
| 水 相 | 三氯乙烷相 | ||||
| 三氯乙烷(S)/% | 水(B)/% | 丙酮(A)/% | 三氯乙烷(S)/% | 水(B)/% | 丙酮(A)/% |
| 0.52 0.60 0.68 0.79 1.04 1.60 3.75 | 93.52 89.40 85.35 80.16 71.33 62.67 50.20 | 5.96 10.00 13.97 19.05 27.63 35.73 46.05 | 90.93 84.40 78.32 71.01 58.21 47.53 33.70 | 0.32 0.60 0.90 1.33 2.40 4.26 8.90 | 8.75 15.00 20.78 27.66 39.39 48.21 57.40 |
试求:
用一单效蒸发器,将2500kg/h的NaOH水溶液由10%浓缩至25%(均为质量分数)。已知加热蒸汽压力为450kPa,蒸发室内压力为101.3kPa(均为绝对压强)。溶液沸点为115℃,比热容为3.9kJ/(kg·℃),蒸发器的热损失为20kW。试计算以下两种情况的加热蒸汽消耗量和单位蒸汽消耗量。
(1)25℃进料;
(2)沸点进料。