 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知(Fe3+/Fe2+)=+0.771V,(/Mn2+)=+1.51V,两电对组成原电池,则______是较强的氧化剂,______是较强的还原剂。
已知


查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知


 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知(Fe3+/Fe2+)=+0.771V,(/Mn2+)=…”相关的问题
更多“已知(Fe3+/Fe2+)=+0.771V,(/Mn2+)=…”相关的问题
已知Θ(Fe3+/Fe2+)=+0.77v,测得(Fe3+/Fe2+)=+0.73v,这说明()。
A.(Fe3+)<1.0mol•L-1
B.(Fe2+)<1.0mol•L-1
C.(Fe3+)/(Fe2+)>1.0
D.(Fe3+)/(Fe2+)<1.0
A.c(Fe3+)<1
B.c(Fe2+)<1
C.c(Fe2+)/c(Fe3+)<1
D.c(Fe3+)/c(Fe2+)<1
将反应2Fe2++3H++


 (Fe3+/Fe2+)>
(Fe3+/Fe2+)> (I2/I-)>
(I2/I-)> (Sn4+/Sn2+),下列物质能共存的是( )。
(Sn4+/Sn2+),下列物质能共存的是( )。A.Fe3+和Sn2+
B.Fe2+和I2
C.Fe3+和I-
D.I2和Sn2+
已知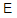 (
(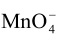 /Mn2+)=1.51V,
/Mn2+)=1.51V,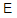 (Fe3+/Fe2+)=0.771V,下列比较正确的是( )。
(Fe3+/Fe2+)=0.771V,下列比较正确的是( )。
A.氧化性: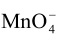 >Fe3+B.氧化性:
>Fe3+B.氧化性: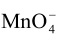 <Fe3+
<Fe3+
C.还原性:Mn2+>Fe2+D.还原性:Mn2+=Fe2+
A.1.01V
B.0.202V
C.0.889V
D.0.771V
已知在1mol·L-1H2SO4溶液中,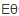 (Ce4+/Ce3+)=1.44V,
(Ce4+/Ce3+)=1.44V,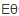 (Fe3+/Fe2+)=0.68V,在此条件下,用Ce(SO4)2标准溶液滴定Fe2+,其化学计量点的电位为______。
(Fe3+/Fe2+)=0.68V,在此条件下,用Ce(SO4)2标准溶液滴定Fe2+,其化学计量点的电位为______。
A.=1
B.>1
C.<1
D.无法确定
通过计算说明,反应 在标准状态时能否自发进行?已知
在标准状态时能否自发进行?已知
