 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
配制I2标准溶液时,必须加入KI,下列叙述正确的是()。
A.防止I-的氧化
B.防止I2挥发,增大I2溶解度
C.操作方便
D.提高I2的氧化能力
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.防止I-的氧化
B.防止I2挥发,增大I2溶解度
C.操作方便
D.提高I2的氧化能力
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“配制I2标准溶液时,必须加入KI,下列叙述正确的是()。”相关的问题
更多“配制I2标准溶液时,必须加入KI,下列叙述正确的是()。”相关的问题
A.n(Ba)=2n(Na2S2O3)
B.n(Ba)=6n(Na2S2O3)
C.n(Ba)=12n(Na2S2O3)
D.n(Ba)=n(Na2S2O3)
A.直接滴定法
B.返滴定法
C.置换滴定法
D.间接滴定法
称取含甲酸(HCOOH)试样0.2040g,溶解于碱性溶液后加入0.2010mol/LKMnO4溶液25.OOmL,待反应完成后,酸化,加入过量的KI还原过剩的

碘在水中的溶解度小,而挥发性强,所以碘标准溶液配制时,将一定量的I2溶于______溶液。
称取含有KI的试样0.5000g,溶于水后先用Cl2水氧化I-为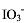 ,煮沸除去过量Cl2;再加入过量KI试剂,滴定I2时消耗了0.02082mol/L Na2S2O321.30mL。计算试样中KI的质量分数。
,煮沸除去过量Cl2;再加入过量KI试剂,滴定I2时消耗了0.02082mol/L Na2S2O321.30mL。计算试样中KI的质量分数。
(提示:反应为CH2OHCH2OH+



I2+

称取含NaIO3和NaIO4的混合试样1.000g,溶解后定容于250mL容量瓶中;准确移取试液50.00mL,调至弱碱性,加入过量KI,此时IO4-被还原为IO3-(IO3-不氧化I-);释放出的I2用0.04000mol/L Na2S2O3溶液滴定至终点时,消耗10.00mL。另移取试液20.00mL,用HCl调节溶液至酸性,加入过量的KI;释放出的I2用0.04000mol/LNa2S2O3溶液滴定,消耗30.00mL。计算混合试样中NaIO3和NaIO4的含量。
A.直接碘量法、间接碘量法均可在酸性、中性或碱性溶液中进行
B.直接碘量法、间接碘量法淀粉指示剂均应在滴定前加入
C.碘量法可在室温下进行,也可在高温下进行
D.过量KI可增大I2的溶解度,降低I2的挥发性,提高淀粉指示剂的灵敏度
溶解0.2000g基准K2Cr2O7,酸化并加入过量的KI,析出的I2用44.80mLNa2S2O3滴定,计算Na2S2O3溶液的浓度。
今有25.00mL KI溶液,用10.00mL0.05000mol/L KIO3溶液处理后,煮沸溶液以除去I2。冷却后,加入过量KI溶液使之与剩余的KIO3反应,然后将溶液调至中性。析出的I2用0.1008mol/L Na2S2O3溶液滴定,用去21.14mL,计算KI溶液的浓度。