 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
甲醇(CH3OH)是一种具有高辛烷值并能完全燃烧的“新型燃料”,可以用氢和煤人工制造。 根据: (1
甲醇(CH3OH)是一种具有高辛烷值并能完全燃烧的“新型燃料”,可以用氢和煤人工制造。 根据: (1)CH3OH(l)+1/2O2(g)=C(石墨)+2H2O(l),△rHΘm=-333.00KJmol-1 (2)C(石墨)+1/2O2(g)=CO(g),△rHΘm=-111.52 kJmol-1 (3)H2(g)+1/2O2(g)——H2O(l),△rHΘm=-285.83 kJmol-1 计算反应(4)2H2(g)+CO(g)=CH3OH(l)的△rHΘm。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“甲醇(CH3OH)是一种具有高辛烷值并能完全燃烧的“新型燃料…”相关的问题
更多“甲醇(CH3OH)是一种具有高辛烷值并能完全燃烧的“新型燃料…”相关的问题
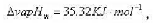 求在上述温度、压力条件下,1Kg液态甲醇全部成为甲醇蒸汽时Q.W,ΔP,ΔH及ΔS。
求在上述温度、压力条件下,1Kg液态甲醇全部成为甲醇蒸汽时Q.W,ΔP,ΔH及ΔS。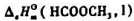 为-979.5kJ·mol-1,甲酸(HCOOH,I)、甲醇(CH3OH,1)、水(H2O,I)及二氧化碳(CO2,g)的标准摩尔生成焓
为-979.5kJ·mol-1,甲酸(HCOOH,I)、甲醇(CH3OH,1)、水(H2O,I)及二氧化碳(CO2,g)的标准摩尔生成焓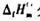 分别为-424.72kJ·mol-1,-238.66kJ·mol-1,-285.83kJ·mol-1及-393.509kJ·mol-1.应用这些数据求25℃时下列反应的标准摩尔反应焓.
分别为-424.72kJ·mol-1,-238.66kJ·mol-1,-285.83kJ·mol-1及-393.509kJ·mol-1.应用这些数据求25℃时下列反应的标准摩尔反应焓.
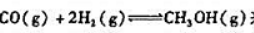 来合成,225℃时该反应的Kθ=6.08x10-3.假定开始时p(CO):p(H2)=1:2,平衡时p(CH3OH)=50.0kPa.计算CO和H2的平衡分压.
来合成,225℃时该反应的Kθ=6.08x10-3.假定开始时p(CO):p(H2)=1:2,平衡时p(CH3OH)=50.0kPa.计算CO和H2的平衡分压. ;
;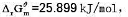 求此反应的
求此反应的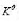 ;
;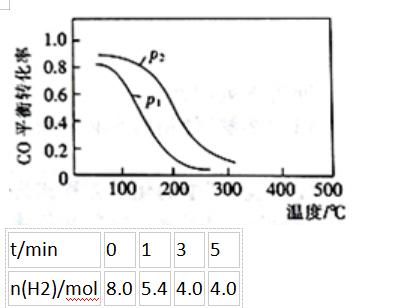 ①△H2()(填“>”“<”或“=”)0。
①△H2()(填“>”“<”或“=”)0。
















