 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
假设某一反应的速率决定步骤是2A(g)+B(g)====C(g)。将2mol A(g)和1mol B(g)放在一容器中混合,反应立刻发生。
假设某一反应的速率决定步骤是2A(g)+B(g)====C(g)。将2mol A(g)和1mol B(g)放在一容器中混合,反应立刻发生。比较下列情况时的反应速率与反应的初速率:
(1)A和B都用掉一半时;
(2)A和B都用掉2/s时。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
假设某一反应的速率决定步骤是2A(g)+B(g)====C(g)。将2mol A(g)和1mol B(g)放在一容器中混合,反应立刻发生。比较下列情况时的反应速率与反应的初速率:
(1)A和B都用掉一半时;
(2)A和B都用掉2/s时。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“假设某一反应的速率决定步骤是2A(g)+B(g)====C(…”相关的问题
更多“假设某一反应的速率决定步骤是2A(g)+B(g)====C(…”相关的问题
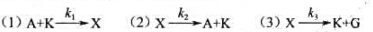 达稳态后,dex/dt=0,求:(1)反应速率-dcA/dt的-般表达式(式中不含X项);(2)k2》k3的反应速率简化表达式:(3)k3>>k2的反应速率简化表达式。
达稳态后,dex/dt=0,求:(1)反应速率-dcA/dt的-般表达式(式中不含X项);(2)k2》k3的反应速率简化表达式:(3)k3>>k2的反应速率简化表达式。
A.0.25倍
B.4倍
C.8倍
D.相等
A.①③
B.①④
C.②③
D.③④
A.总包反应的表观速率由处于中间的步骤的速率所决定;
B.总包反应的表观速率由第一步骤速率所决定;
C.总包反应的表观速率由最后一步速率所决定;
D.总包反应的表观速率由最难进行的步骤速率所决定
非常富电子芳环的硝化是扩散控制的。虽然 反应活性很高,这些反应有时表现出好的加成区域选择性。提出假设机理中每步反应的相对速率,为了解释化学反应性和选择性之间似乎缺乏的关系,预测哪些步骤反应是可逆的。
反应活性很高,这些反应有时表现出好的加成区域选择性。提出假设机理中每步反应的相对速率,为了解释化学反应性和选择性之间似乎缺乏的关系,预测哪些步骤反应是可逆的。
反应2NO(g)+H2(g)→N2O(g)+ H2O(g)的速率方程为

反应在恒温、恒容的条件下进行,测得实验数据如下:
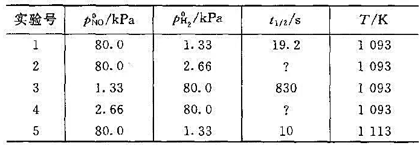
(1)求所缺的半衰期数据;(2)求1093 K时的速率常数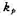 ;(3)求反应的活化能
;(3)求反应的活化能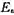 ;(4)提出一个只涉及双分子步骤的反应机理,由此机理可得上述规律;(5)如果1093K时,
;(4)提出一个只涉及双分子步骤的反应机理,由此机理可得上述规律;(5)如果1093K时,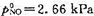 ,
,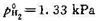 ,求该反应的半衰期。
,求该反应的半衰期。
一定温度下,对反应2A====B+D,实验测定了如下数据:
cA/(mol·L-1) 0.40 0.20
速率/(mol·L-1·min-1) 0.02 0.01
则该反应的速率方程为r=______,速率常数k=______。
A.气体总质量不变
B.混合气体密度不变
C.反应物B的浓度不变
D.混合气体平均相对分子质量不再改变