 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
反应 已达到化学平衡状态,若升高温度,生成物C的浓度增加,则逆反应是( )
已达到化学平衡状态,若升高温度,生成物C的浓度增加,则逆反应是( )
A.放热反应
B.吸热反应
C.没有明显的热效应
D.无法判断
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 已达到化学平衡状态,若升高温度,生成物C的浓度增加,则逆反应是( )
已达到化学平衡状态,若升高温度,生成物C的浓度增加,则逆反应是( )A.放热反应
B.吸热反应
C.没有明显的热效应
D.无法判断
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“反应已达到化学平衡状态,若升高温度,生成物C的浓度增加,则逆…”相关的问题
更多“反应已达到化学平衡状态,若升高温度,生成物C的浓度增加,则逆…”相关的问题
已知可逆反应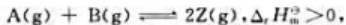 在温度T时达到了化学平衡。若采取下列措施,可能使化学平衡向正反应方向移动的是()。
在温度T时达到了化学平衡。若采取下列措施,可能使化学平衡向正反应方向移动的是()。
A、保持原来的温度
B、升高温度
C、降低温度
D、压缩系统的体积,以增大总压力
A.可逆反应的特征是正反应速率和逆反应速率相等
B.在其它条件不变时,升高温度可以使化学平衡向放热反应的方向移动
C.在其它条件不变时,增大压强一定会破坏气体反应的平衡状态
D.在其它条件不变时,使用催化剂可改变化学反应速率,但不能改变化学平衡状态
A.种物质的的浓度相等
B.正、逆反应速率相等且不于零
C.四种物质在容器中共存
D.四种物质的浓度均不再改变
A.升高温度可使化学平衡向正反应方向移动
B.#图片1$#
C.反应物的分压等于生成物的分压
D.加入催化剂,可使化学平衡向正反应方向移动
反应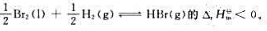 上述可逆反应达到化学平衡后,降低温度时,平衡()移动:缩小容器的体积增大压力时,平衡()加入催化剂时,标准平衡常数()移动;升高温度时,标准平衡常数()。
上述可逆反应达到化学平衡后,降低温度时,平衡()移动:缩小容器的体积增大压力时,平衡()加入催化剂时,标准平衡常数()移动;升高温度时,标准平衡常数()。
若 298K 时反应N2O4 (g) = 2NO2(g) 的 Kө =0.1132,则当 N2O4 和 NO2 的分压均为1.0 kPa 时, 该反应()
A向生成 NO2 的方向进行
B向生成 N2O4 的方向进行
C正好达到化学平衡
D难于判断其进行方向
碳与氧间发生的有关反应如下:
(A)

(B)
(C)

反应(B)的


