 更多“在同一温度下,饱和蒸气压高的物质()”相关的问题
更多“在同一温度下,饱和蒸气压高的物质()”相关的问题
易挥发组分A和难挥发绢分B的饱和蒸气压数据如下。
温度/℃ | 组分A的饱和蒸气压 p_{A}^{0}/mmHg | 组分B的饱和蒸气压 p_{B}^{0}/mmHg |
74 76 78 80 82.5 | 100 107 116 125 135.8 | 71 77 84 92 100 |
试求A、B混合液在100mmHg下的(1)相对挥发度;(2)不同温度下组分A中液相摩尔分数;(3)不同温度下组分A中气相摩尔分数;(4)两组分的平衡方程式。
A(I)与B(I)形成理想液态混合物.温度T下,纯A(I)的饱和气压为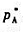 ,纯B(I)的饱和蒸气压为
,纯B(I)的饱和蒸气压为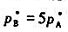 .在同样温度下,将A(I)与B(I)混合形成,气-液平衡系统,测得其总压为2
.在同样温度下,将A(I)与B(I)混合形成,气-液平衡系统,测得其总压为2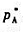 .此平衡系统气相中B的摩尔分数yB=().(填入具体数值)
.此平衡系统气相中B的摩尔分数yB=().(填入具体数值)
假设某气体在固体表面上吸附平衡时的压力p,远远小于该吸附质在相同温度下的饱和蒸气压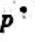 .试由BET公式:
.试由BET公式:
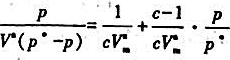
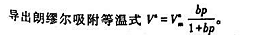
水的饱和蒸气压为2.800kPa).试求:
(1)23℃时该气体中氢气的分压;
(2)氢气的物质的量;
(3)若在收集氢气之间,集气瓶中已充有氮气20.0mL,其温度也是23℃,压力为100.5kPa:收集氢气之后,气体的总体积为390.0mL.计算此时收集的氢气分压,与(2)相比,氢气的物质的量是否发生变化?
已知水(H2O,I)在100℃的饱和蒸气压p=101.325kPa,在此温度.压力下水的摩尔蒸发焓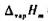 =40.668kJ·mol-1.求在100℃,101.325kPa下使1kg水蒸气全部凝结成液体水时的Q,W,ΔU和ΔH.设水蒸气适用理想气体状态方程.
=40.668kJ·mol-1.求在100℃,101.325kPa下使1kg水蒸气全部凝结成液体水时的Q,W,ΔU和ΔH.设水蒸气适用理想气体状态方程.
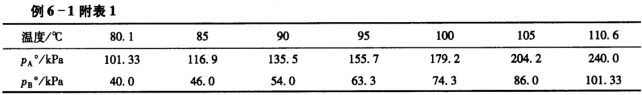
苯(A)与甲苯(B)的饱和蒸气压和温度的关系数据如例6—1附表1所示。试利用拉乌尔定律和相对挥发度,分别计算苯一甲苯混合液在总压p为101.33kPa下的气液平衡数据,并作出温度—组成图。该溶液可视为理想溶液。
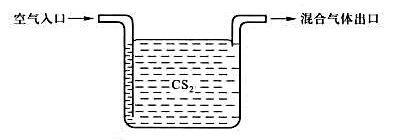
用饱和气流法测CS2的蒸气压。293K,100kPa下,使3.00dm3干燥空气缓慢通过如图所示的CS2计泡器,带走6.24gCS2。试计算该温度下CS2,的饱和蒸气压。


 如果结果不匹配,请
如果结果不匹配,请 

















