 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
一定温度下.纯液休A的饱和热气(压为pi,化学势为i凝固点为T",当A中加入少量不挥发性溶质后,上.述千个量为pnfn. Tr,它们的关系为( )
A、
B、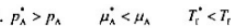
C、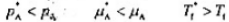
D、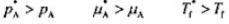
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A、
B、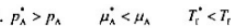
C、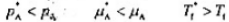
D、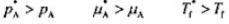
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“一定温度下.纯液休A的饱和热气(压为pi,化学势为i凝固点为…”相关的问题
更多“一定温度下.纯液休A的饱和热气(压为pi,化学势为i凝固点为…”相关的问题
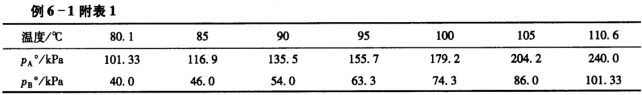
苯(A)与甲苯(B)的饱和蒸气压和温度的关系数据如例6—1附表1所示。试利用拉乌尔定律和相对挥发度,分别计算苯一甲苯混合液在总压p为101.33kPa下的气液平衡数据,并作出温度—组成图。该溶液可视为理想溶液。
物料中非结合水分的特点之一是其产生的水蒸气压( )同温度下纯水的饱和蒸气压。
A.大于 B.小于 C.等于
在一定温度下,将1.0molNa2O2(g)放入一密闭容器中,发生下列可逆反应
 当达到化学平衡时,容器内有0.8molNO,气体总压为100kPa。则该可逆反应在此温度下的标准平衡常数为().
当达到化学平衡时,容器内有0.8molNO,气体总压为100kPa。则该可逆反应在此温度下的标准平衡常数为().
A、0.40
B、0.67
C、0.76
D、1.3
在一单效中央循环管式蒸发器内将浓度10%(质量分数,下同)的NaOH溶液浓缩到40%。二次蒸汽绝对压强为40kPa,相应的饱和温度为75℃。已知在操作压强下蒸发纯水时,液柱中部的沸点温度为80℃。试求溶液的沸点及由于溶液静压强引起的温度差损失。
10%及40%NaOH水溶液杜林线的斜率及截距如下:
| 斜率 | 截距 | |
10% 40% | 1.02 1.11 | 4.5 34 |
易挥发组分A和难挥发绢分B的饱和蒸气压数据如下。
温度/℃ | 组分A的饱和蒸气压 p_{A}^{0}/mmHg | 组分B的饱和蒸气压 p_{B}^{0}/mmHg |
74 76 78 80 82.5 | 100 107 116 125 135.8 | 71 77 84 92 100 |
试求A、B混合液在100mmHg下的(1)相对挥发度;(2)不同温度下组分A中液相摩尔分数;(3)不同温度下组分A中气相摩尔分数;(4)两组分的平衡方程式。
某温度下,将一定瓜周体NHI4HS置于一真空容器中,它将按下式分解:
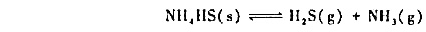
平衡时总I为68.0kPa。
(1)计算该分解反应的Kθ;
(2)保持温度不变,缓缓加入NH3直至NH3的平衡分压为93.0kPa,则此时H2S分正是多少?体系的总压是多少?
某温度下,
 反应达到平衡,若增大或减少B的量,C和A的平衡浓度都不变,则B是 ()
反应达到平衡,若增大或减少B的量,C和A的平衡浓度都不变,则B是 ()
A.纯固体或纯液体
B.气体
C.溶液
D.以上都正确