 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在温度T时,某化学反应的ΔrHmθ< 0,δrgmθ >0,此时该反应的平衡常数Kθ应是()
A.Kθ>1,且随温度升高而增大
B.Kθ>1,且随温度升高而减小
C.Kθ<1,且随温度升高而增大
D.Kθ<1,且随温度升高而减小
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.Kθ>1,且随温度升高而增大
B.Kθ>1,且随温度升高而减小
C.Kθ<1,且随温度升高而增大
D.Kθ<1,且随温度升高而减小
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在温度T时,某化学反应的ΔrHmθ0,此时该反应的平衡常数K…”相关的问题
更多“在温度T时,某化学反应的ΔrHmθ0,此时该反应的平衡常数K…”相关的问题
n0mol的气体A1和n0mol的气体A2的混合物在温度T和压强p下所占的体积为V0,当发生化学反应ν3A3+ν4A4-ν1A1-ν2A2=0,并在相同的温度和压强下达到平衡时,其体积为Ve.试证明:反应度ξ可表示为
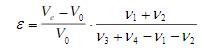
反应2NaHCO3(s)===Na2CO3(s)+H2O(g)+CO2(g)在不同温度时的平衡总压如表5-3所示。
表5-3 | ||||||
t/℃ | 30 | 50 | 70 | 90 | 100 | 110 |
p/kPa | 0.827 | 3.999 | 15.90 | 55.23 | 97.47 | 167.0 |
设反应的Δr Hm与温度无关。
求:(1)上述反应的ΔrHm;
(2)lg(p/kPa)与T的函数关系;
(3)NaHCO3(s)的分解温度。
n0v1mol的气体A1和n0ν2mol气体A2的混合物在温度T、压强p下所占体积为V0,当发生化学反应
并在同样的温度和压强下达到平衡时,其体积为Ve,证明反应度ε为

电池Mo(S)|MoS2(S)|H2S(100kPa)|KCl(0.01mol/kg)|HCl(0.01mol/kg)|H2(100kPa)|Pt,测得其在不同温度下的电池电动势数据为 T/K 288 298 308 E/V 0.4148 0.4119 0.4087 (1)写出电极反应和电池反应; (2)由题给数据推导出电池反应的平衡常数与温度的关系式,并计算△rHm; (3)用电化学方法计算298K时电池反应的△rSm,将其与热力学方法计算所得结果相比较可得出什么结论?298K时,物质的规定熵数据为 物质 H(g)H2S(g) Mo(s) MoS2(s) Sm/[J/(K.mol)] 130.6 205.6 28.58 62.59
A.正、逆反应速率均减小
B.正反应速率减小;逆反应速率增大
C.正、逆反应速率均增大
D.正反应速率增大;逆反应速率减小