 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知298.15K时,,,标准态时:(1)写出原电池符号(应自发进行);(2)写出电极反应及电池反应;(3)计算原电池的;(4)
已知298.15K时, ,
, ,标准态时:(1)写出原电池符号(应自发进行);(2)写出电极反应及电池反应;(3)计算原电池的
,标准态时:(1)写出原电池符号(应自发进行);(2)写出电极反应及电池反应;(3)计算原电池的 ;(4)计算电池反应的
;(4)计算电池反应的 ;(5)求AgI的Ksp。
;(5)求AgI的Ksp。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知298.15K时, ,
, ,标准态时:(1)写出原电池符号(应自发进行);(2)写出电极反应及电池反应;(3)计算原电池的
,标准态时:(1)写出原电池符号(应自发进行);(2)写出电极反应及电池反应;(3)计算原电池的 ;(4)计算电池反应的
;(4)计算电池反应的 ;(5)求AgI的Ksp。
;(5)求AgI的Ksp。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知298.15K时,,,标准态时:(1)写出原电池符号(应…”相关的问题
更多“已知298.15K时,,,标准态时:(1)写出原电池符号(应…”相关的问题
(I)的标准摩尔生成焓分别为-394kJ·mol-1和-286kJ·mol-1计算C2H5OH(1)在298.15K时的标准摩尔生成焓。
试求298.15K时,下述反应的KaΘ CH3COOH(1)+C2H5OH(1)==CH3COOC2H5(1)+H2O(1)已知各物质的标准生成自由能△fGmΘ。 物质 △fGmΘ(kJ/mol) CH3COOH(1) 一389.9 CH3COOC2H5(1) 一332.55 H2O(1) 一237.129 C2H5OH(1) 一168.49
298.15K时,已知下列热化学方程式
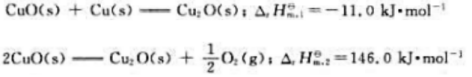
则298.15K时,CuO(s)的标准摩尔生成焓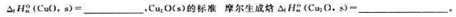
已知下列反应在298.15K的平衡常数:
(1)SnO2(s)+2H2(g) 2H2O(g)+Sn(s)
2H2O(g)+Sn(s)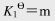
(2)H2O(g)+CO(g) H2(g)+CO2(g);
H2(g)+CO2(g);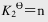
计算反应2CO(g)+SnO2(s) Sn(s)+2CO2(g)在298.15K时的平衡常数KΘ3。
Sn(s)+2CO2(g)在298.15K时的平衡常数KΘ3。
已知四氧化二氮的分解反应为N2O4(g)===2NO2(g)。在298.15K时,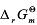 =4.75kJ·mol-1。试判断在此温度及下列条件下,反应进行的方向。
=4.75kJ·mol-1。试判断在此温度及下列条件下,反应进行的方向。
(1)N2O4(g,100kPa),NO2(g,100kPa);
(2)N2O4(g,1000kPa),NO2(g,100kPa);
(3)N2O4(g,300kPa),NO2(g,200kPa)。
A.在温度升高至一定数值以上即可自发进行
B.在温度降低至一定数值以上即可自发进行
C.在任何温度下反应都能自发进行
D.在任何温度下反应都不能自发进行
A.2.9×103kJ·mol-1
B.-114kJ·mol-1
C.-110kJ·mol-1
D.-13.9kJ·mol-1
已知298.15K时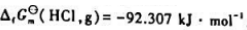 化学反应
化学反应
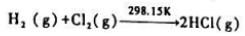
在催化剂的作用下反应速率大大加快时,反应的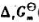 (298.15K)=().
(298.15K)=().