 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[不定项选择题]
常温下已知两种一元弱酸HX和HY,如果向NaX溶液中通入少量CO2气体生成HX和NaHCO3;往NaY溶液中通入少量CO2生成HY和Na2CO3。下列有关叙述正确的是()。
A.酸性由强至弱:HX>HY>H2CO3
B.结合H+的能力:Y->CO32->X->HCO3-
C.溶液碱性:NaX>Na2CO3>NaY>NaHCO3
D.4NaX溶液中通入足量CO2后的离子浓度:c(Na+)>c(HCO3-)>c(X-)>c(OH-)>c(H+)
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“常温下已知两种一元弱酸HX和HY,如果向NaX溶液中通入少量…”相关的问题
更多“常温下已知两种一元弱酸HX和HY,如果向NaX溶液中通入少量…”相关的问题
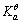 值。
值。
















