 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
以NaOH滴定H3PO4(ka1=7.5×10-3,ka2=6.2×10-8,ka3=5.0×10-13)至生成Na2HPO4时,溶液的pH值应当是()。
A.4.7
B.8.7
C.9.8
D.10.7
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.4.7
B.8.7
C.9.8
D.10.7
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“以NaOH滴定H3PO4(ka1=7.5×10-3,ka2=…”相关的问题
更多“以NaOH滴定H3PO4(ka1=7.5×10-3,ka2=…”相关的问题
 =7.5×10-3,
=7.5×10-3, =6.2×10-8,
=6.2×10-8, =5×10-13)至生成NaH2PO4时溶液的pH为( )。
=5×10-13)至生成NaH2PO4时溶液的pH为( )。A.2.3
B.2.6
C.3.6
D.4.7
E.9.2
A.V1=V2
B.V1>V2
C.V1<V2
D.V1=2V2
E.V2=2V1
B.NaOH滴定H3PO4至pH为5.5时(第一计量点)
C.蒸馏法测NH4+时,用HCl吸收NH3,以NaOH标准液返滴定pH=7.0
D.HCl滴定NaOH,用酚酞为指示剂
NaOH标准溶液滴定H3PO4至甲基红终点时的质子条件式是( )。
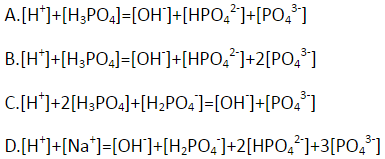
A.偏高
B.偏低
C.无影响
D.不能确定
E.全部不对
A.2.00
B.3.00
C.10.00
D.20.00
E.30.00
A.甲基橙(pH变色范围:3.1~4.4)
B.甲基红(pH变色范围:4.2~6.2)
C.溴酚蓝(pH变色范围:5.2~7.0)
D.酚酞(pH变色范围:8.0~10.0)
E.麝香草酚蓝加酚红(pH变色点:7.5)
称取磷肥2.500g,萃取其中有效P2O5,制成250mL试液,将其中H3PO4沉淀为磷钼酸喹啉。沉淀分离后,洗涤至中性,然后加0.2500mol/L NaOH溶液25.00mL使沉淀溶解,以0.25000mol/L HCl溶液回滴,用去3.25mL。计算磷肥中P2O5的含量。
(C9H7N)3H3[PO4·12MoO3]·H2O+26NaOH→
Na2HPO4+12Na2MoO4+3C9H7N+15H2O
把某一纯一元弱酸HA0.5000g溶于40.00mL水后,以0.1000mol/L NaOH溶液滴定。从滴定曲线上得知V(NaOH)=20.00mL时溶液pH=4.21,V(NaOH)=40.00mL时达到化学计量点。问: