更多“给出25℃时下列电池的①电动势;②正,负极和阴,阳极。”相关的问题
更多“给出25℃时下列电池的①电动势;②正,负极和阴,阳极。”相关的问题
用镁离子选择电极测定溶液中的Mg2+,其电池的组成为
镁离子选择电极|Mg2+||饱和甘汞电极
在25℃时,c(Mg2+)=1.15×10-2mol·L-1时,该电池的电动势为0.275V,当用Mg2+试液代替已知溶液时,测得电动势为0.280V,计算试液的pMg。
已知

Cd|Cd2+(0.10mol·L-1)||Sn4+(0.10mol·L-1),Sn2+(0.0010mol·L-1)|Pt在298K时的电动势ε,并写出电池反应,标明正、负极。
A.5×2.73F
B.-5×2.73F
C.10×2.73F
D.-10×2.73F
已知反应
2Cr3++3Cl2+7H2O=Cr2O72-+6C1-+14H+
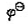 (Cr2O72-/Cr3+)=1.33V,
(Cr2O72-/Cr3+)=1.33V,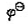 (Cl2/CI-)=1.36V,F=95500J·V-1·mol-2若在298K时组成原电池。
(Cl2/CI-)=1.36V,F=95500J·V-1·mol-2若在298K时组成原电池。
(1)写出该原电监的电池符号,并计算标准电动势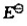 ;(2)计算
;(2)计算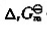 (298K)并判断反应进行的方向;(3)计算标准平衡常数
(298K)并判断反应进行的方向;(3)计算标准平衡常数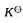 ;(4)若c(H+)=10mol·dm-3,其他离子浓度均为标准浓度,求原电池的电动势E并判断反应进行的方向
;(4)若c(H+)=10mol·dm-3,其他离子浓度均为标准浓度,求原电池的电动势E并判断反应进行的方向
A.为防止食物油脂酸化而加入的没食子酸正丙酯
B.在分解氯酸钾制备氧气实验时加入的二氧化锰
C.在用锌和稀硫酸反应制备氧气时加入的硫酸铜
D.在大雪后为促使积雪融化而在马路上撒下的盐
已知下列反应△rHΘm值的正、负,判断反应在高温和低温时的自发状态。 (1)2Fe(S)+3/2O2(g)=Fe2O3(s) △rHΘm<0 (2)2NH3(g)=N2(g)+3H2(g) △rHΘm>0 (3)C2H5OH(1)=C2H5OH(g) △rHΘm>0 (4)2Cl2(g)+7O2(g)=2Cl2O7(l) △rHΘm>0 (5)C2H5OH(l)+2O2(g)=2CO2(g)+3H2O(g) △rHΘm<0


 如果结果不匹配,请
如果结果不匹配,请