 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在0.1mol·L-1HCl溶液中,用Fe3+滴定Sn2+,其反应为:2Fe3++Sn2+=2Fe2++Sn4+(1)计算下列反应的化
在0.1mol·L-1HCl溶液中,用Fe3+滴定Sn2+,其反应为:
2Fe3++Sn2+=2Fe2++Sn4+
(1)计算下列反应的化学计量点的电位和滴定到99.9%和100.1%时的电位。
(2)计算平衡常数及讨论反应进行的完全程度。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在0.1mol·L-1HCl溶液中,用Fe3+滴定Sn2+,其反应为:
2Fe3++Sn2+=2Fe2++Sn4+
(1)计算下列反应的化学计量点的电位和滴定到99.9%和100.1%时的电位。
(2)计算平衡常数及讨论反应进行的完全程度。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在0.1mol·L-1HCl溶液中,用Fe3+滴定Sn2+,…”相关的问题
更多“在0.1mol·L-1HCl溶液中,用Fe3+滴定Sn2+,…”相关的问题
标定0.1mol·L-1HCl,欲消耗HCl溶液25mL左右,计算应称取Na2CO3基准物的质量。若改用硼砂(Na2B4O7·10H2O)为基准物,结果又如何?已知Na2CO3的摩尔质量为106.0g·mol-1,Na2B4O7·10H2O的摩尔质量为381.4g·mol-1。
在H3PO4存在下的HCl溶液中,用0.1mol/LK2Cr2O7溶液滴定0.1mol/L Fe2+溶液时,已知化学计量点的电位为0.86V。最合适的指示剂为( )。
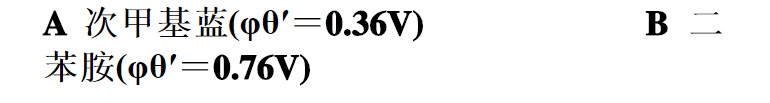
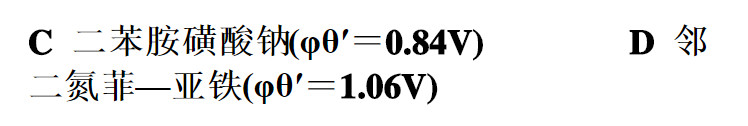
称取烧碱试样2.6830g,加水溶解,转入250mL的容量瓶中定容。吸取25.00mL该溶液,用0.09918mol·L-1HCl溶液滴定至终点,用去盐酸20.32mL,计算试样中氢氧化钠的质量分数。已知氢氧化钠的摩尔质量为40.00g·mol-1。
含有NaOH和Na2CO3以及中性杂质的试样0.2000g,用0.1000mol·L-1HCl溶液22.20mL滴定至酚酞终点,继续用HCl滴定至甲基橙终点,又用去12.20mL,计算试样中NaOH和Na2CO3的质量分数。
蛋白质样品0.2318g消解后,加碱蒸馏,用4% H3BO3溶液吸收蒸馏出的NH3,然后用0.1200mol·L-1HCl 21.60mL滴定至终点。计算样品中N的质量分数。
含有NaHCO3和Na2CO3以及中性杂质的样品1.200g溶于水后,用15.00mL 0.5000mol·L-1HCl溶液滴定至酚酞终点。继续滴定至甲基橙终点又用去HCl 22.00mL。计算样品中NaHCO3和Na2CO3的质量分数。
(1)试液中所含的NaOH和Na2CO3的物质的量相同;
(2)试液中所含的NaHCO3和Na2CO3的物质的量相同;
(3)加入甲基橙时.试液呈终点颜色。前两种情况下,若继续以甲基橙为指示剂,还需要加入多少毫升HCl溶液才能滴定至终点?第三种情况的试液组成如何?
重0.7000g的试样(含有Na3PO4、Na2HPO4或NaH2PO4及不与酸作用的杂质),溶于水后用甲基红作指示剂,以0.5000mol·L-1HCl溶液滴定,耗酸14.00mL。同样质量的试样,用酚酞作指示剂,需0.5000mol·L-1HCl溶液5.00mL滴定至终点。计算试样中杂质的含量。