 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
细胞内含有0.140mol·L-1的KCl和0.010mol·L-1的NaCl,在细胞膜外是0.145mol·L-1的NaCl和0.005mol·L-1的KCl。在
细胞内含有0.140mol·L-1的KCl和0.010mol·L-1的NaCl,在细胞膜外是0.145mol·L-1的NaCl和0.005mol·L-1的KCl。在37℃体温条件下:
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
细胞内含有0.140mol·L-1的KCl和0.010mol·L-1的NaCl,在细胞膜外是0.145mol·L-1的NaCl和0.005mol·L-1的KCl。在37℃体温条件下:
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“细胞内含有0.140mol·L-1的KCl和0.010mol…”相关的问题
更多“细胞内含有0.140mol·L-1的KCl和0.010mol…”相关的问题
 的Kc=3.6×10-3,此时,CO2的平衡浓度是( )mol·L-1。
的Kc=3.6×10-3,此时,CO2的平衡浓度是( )mol·L-1。A.3.6×10-3
B.1/(3.6×10-3)
C.(3.6×10-3)1/2
D.(3.6×10-3)2
 的Kc=45.9,各物质以起始浓度c(H2)=0.0600mol·L-1、c(I2)=0.4000mol·L-1、c(HI)=2.00mol·L-1进行混合,在上述温度下,反应自发进行的方向是( )。
的Kc=45.9,各物质以起始浓度c(H2)=0.0600mol·L-1、c(I2)=0.4000mol·L-1、c(HI)=2.00mol·L-1进行混合,在上述温度下,反应自发进行的方向是( )。A.自发向右进行
B.自发向左进行
C.反应处于平衡状态
D.反应不发生
反应 在某温度T时,Kc=9.0。若CO和H2O的起始浓度皆为0.02mol·L-1,计算平衡时各物质的浓度和CO的平衡转化率。
在某温度T时,Kc=9.0。若CO和H2O的起始浓度皆为0.02mol·L-1,计算平衡时各物质的浓度和CO的平衡转化率。
哺乳动物的胃壁细胞分泌的HCl浓度达到0.15mol·L-1,分泌的质子由细胞内碳酸酐酶催化CO2水合产生的,然后通过(H+-K+)-ATP酶反向转运泵出,但还需要一个K+-Cl-协同转运蛋白完成整个转运过程。
在0.01mol·L-1[Ag(NH3)2]+溶液中,含有过量的0.01mol·L-1氨水,计算溶液中的Ag+浓度。已知Kf([Ag(NH3)2]+)=1.6×107。
某溶液含有Pb2+和Ba2+,其浓度分别为0.01mol·L-1和0.1mol·L-1,加入K2CrO4溶液后,哪一种离子先沉淀?
含有0.1mol·L-1的Fe3+和Mg2+溶液,用NaOH使两种离子分离,即Fe3+发生沉淀,而Mg2+留在溶液中,溶液pH必须控制在什么范围内?
计算pH=3.0,含有未配位EDTA浓度为0.10mol•L-1时,Fe3+/Fe2+电对的条件电势。(已知pH=3.0时,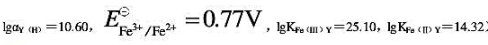 )。
)。
某溶液含有Ba2+、EDTA和


| pH | 8.9 | 9.1 | 9.3 | 9.5 | 9.7 | 10.0 |
| lgY(H) | 1.38 | 1.2 | 1.0 | 0.80 | 0.70 | 0.45 |
含有Na2HPO4.12H2O和NaH2PO4.H2O的混合试样0.6000g,用甲基橙作指示剂,以
0.1000mol·L-1的HCl溶液14.00ml滴定至终点;同样量的试样,用酚酞作指示剂时,需用5.00ml0.1200 mol ·L-1的NaOH滴到终点,计算各组分的百分含量。[已知M (Na2HPO4.12H2O)=358.1g·mol-1,M(NaH2PO4.H2O)=160.0g·mol-1]