 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在一定条件下,反应H2(g)+Br2((g)→2HBr(g)的速率方程符合速率方程的一般形式,即.在某
在一定条件下,反应H2(g)+Br2((g)→2HBr(g)的速率方程符合速率方程的一般形式,即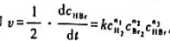 .
.
在某温度下,当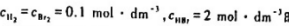 时,反应速率为v.其他不同浓度时的速率如下表所示:
时,反应速率为v.其他不同浓度时的速率如下表所示:

求反应的分级数n1、n2、n3.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在一定条件下,反应H2(g)+Br2((g)→2HBr(g)的速率方程符合速率方程的一般形式,即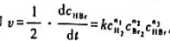 .
.
在某温度下,当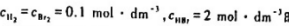 时,反应速率为v.其他不同浓度时的速率如下表所示:
时,反应速率为v.其他不同浓度时的速率如下表所示:

求反应的分级数n1、n2、n3.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在一定条件下,反应H2(g)+Br2((g)→2HBr(g)…”相关的问题
更多“在一定条件下,反应H2(g)+Br2((g)→2HBr(g)…”相关的问题
A. 化学平衡状态是正逆反应都停止的状态
B. 对于可逆反应C(s)+ H20(g) = CO(g) + H2(g),在一定温度下达到平衡,ρ(H20)=ρ(CO)=ρ(H2) ,即反应物与生成物压力相等
C. 反应N2(g) +02(g) =2NO(g)和2N2(g) +202(g) =4NO(g)虽代表同一反应,但是它们的标准平衡常数不相等
D. 多步反应的总标准平衡常数为各步反应标准平衡常数之和
一定条件下反应2NO(g)+O2(g) 2NO2(g)达到平衡.已知该反应的
2NO2(g)达到平衡.已知该反应的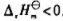 .若保持温度不变、增大压力,则平衡();若保持温度、体积不变,加入惰性组分,则平衡();若保持压力不变、降低温度,则平衡().(选择填入:向左移动、向右移动、不发生移动.)
.若保持温度不变、增大压力,则平衡();若保持温度、体积不变,加入惰性组分,则平衡();若保持压力不变、降低温度,则平衡().(选择填入:向左移动、向右移动、不发生移动.)
17一1 由乙炔制取ClBrCH一CH2Br,下列方法可行的是()。
A.先与HBr加成后再与HCl加成
B.先与H2完全加成后再与Cl2、Br2发生取代反应
C.先与HCl加成后再与Br2加成
D.先与Cl2加成后再与HBr加成
 的Kp=4×10-2,则反应HBr(g)
的Kp=4×10-2,则反应HBr(g) 1/2H2(g)+1/2 Br2(g)的Kp是( )。
1/2H2(g)+1/2 Br2(g)的Kp是( )。A.1/(4×10-2)
B.1/[(4×10-2)1/2]
C.(4×10-2)1/2
D.2×10-1
A.Ag+(aq)+Br-(aq)→AgBr(s)
B.2Ag(s)+Br2(g)→2AgBr(s)
C.Ag(s)+1/2Br2(1)→AgBr(s)
D.Ag(s)+1/2Br2(g)→AgBr(s)
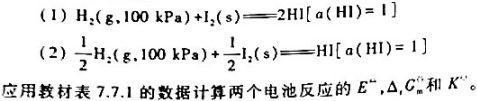
H2O2+Br2+2H+==2Br-+O2
作用10min后,赶去过量的Br2,再以0.3162mol·L-1溶液滴定上述反应产生的H+.需17.08mL达到终点,计算瓶中H2O2的含量(以g/100mL表示).
化合物A(C7H8O)不与Na反应,与浓HI反应生成B和C,B能溶于NaOH,并与FeCl3显紫色,C与AgNO3/乙醇作用,生成AgI沉淀,试推测A、B、C结构。
9. 化合物A(C6H14O)可溶于H2SO4,与Na反应放出H2,与H2SO4共热生成B(C6H12),B可使Br2/CCl4褪色,B经强氧化只生成一种物质C(C3H6O)。试确定A、B、C的结构。
℃下,每升气体会产生3.5×1029次·s-1的碰撞,如果每次碰撞都会发生化学反应,试计算HI的分解反应的速率.实验测定,该反应实际的反应速率是1.2×10-8·mol·dm-3·s-1,试求HI气体中活化分子的百分数(设每次活化分子的相互碰撞都产生反应).
合成氨所用H2的一般制法为:让H2O(g)先通过1000℃以上的煤炭,生成水煤气(CO和H2的混合气体),然后再让H2O(g)和水煤气在400℃左右催化生成更多的H2。写出有关的反应方程式。
煤和由煤与水蒸气反应[C(s)+H2O(g)=H2(g)+CO(g)]而得的水煤气(CO与H2等物质的混合物)都可用做燃料。设煤含碳80%,其余可燃成分忽略不计。试通过计算说明,在实际应用中以水煤气代替煤作燃料的优点。(提示:在任何能量转换过程中,总会有一些能量变成热而扩散到环境中。例如,欲往某体系输入xkJ的能量,实际上提供的热量要远多于该值。)