 更多“新鲜原料最终反应深度的高低用总转化率的大小表示。()”相关的问题
更多“新鲜原料最终反应深度的高低用总转化率的大小表示。()”相关的问题
第1题
煤气产率的高低决定于原料煤的水分、挥发分、固定碳含量等,也与碳转化率有关。挥发分含量愈高,
煤气产率愈____________________ ;原料煤固定碳含量愈高,则煤气产率愈____________________
点击查看答案
第2题
当充填新催化剂的绝热床反应器进口原料温度控制为460℃时,出口物料温度为437℃,转化率符合要求;操作数月后,催
化剂的活性下降。为了保持所要求的转化率,将原料进口温度提高至470℃,出口物料温度相应升至448℃;若反应的活化能为83.7kJ/mol,试估计催化剂活性下降的百分数。
第3题
某反应,当升高反应温度时,反应物的转化率减小,若只增加体系总压时,反应物的转化率提高,则此反应为______热
反应,且反应物分子数______(“大于”、“小于”)产物分子数。
点击查看答案
第4题
以邻甲基环己烯甲醛为原料(A),以异丙醇铝的苯溶液为催化剂,合成双烯201(B),反应可写为2A→B,A的初始浓度为2.
以邻甲基环己烯甲醛为原料(A),以异丙醇铝的苯溶液为催化剂,合成双烯201(B),反应可写为2A→B,A的初始浓度为2.00mol·dm-1,在28℃进行反应,测得反应时间与A的转化率αA的关系如下表:
| t/h | 0 | 3 | 6 | 9 | 12 |
| αA | 0 | 0.46 | 0.63 | 0.72 | 0.77 |
试确定反应的速率方程式。
第6题
惰性气体对化学平衡的影响,描述错误的是()。
A.惰性气体不影响热力学平衡常数值
B.加入惰性气体相当于增加反应系统的总压力
C.对于气体分子数增加的反应,加入水气或氮气,会使反应物转化率提高,使产物的含量增加
D.对于气体分子数增加的反应,加入水气或氮气,使产物的含量增加
第7题
催化剂的活性是衡量催化剂效能大小的标准,在工业上往往用反应物的转化率表示或用一特定反应达到规定的转化率所需要的反应条件来表示,即达到同样的转化率时,反应温度和压力越低,(),催化剂活性越高。
A.反应器体积越小
B.催化剂装填量越小
C.空速越大
D.空速越小
第8题
某温度时8.0mol SO2和4.0mol O2在密闭容器中进行反应生成SO3气体,测得起始时和平衡时(温度不变)系统的总压
某温度时8.0mol SO2和4.0mol O2在密闭容器中进行反应生成SO3气体,测得起始时和平衡时(温度不变)系统的总压力分别为300kPa和220kPa。利用上述实验数据计算该温度时反应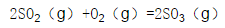 的平衡常数和SO2的转化率。
的平衡常数和SO2的转化率。
第11题
光氧化技术在水处理中有几个明显的优势,不包括以下哪种?()
A.能量来源绿色可持续,可利用太阳光作为能源活化光催化剂
B.氧化性强,可使有机物完全矿化,最终产物是CO2和H2O等无机物
C.处理对象具有特异性,对特定污染物的氧化效果好
D.属于低温深度反应,可以在室温下将有机污染物氧化


 如果结果不匹配,请
如果结果不匹配,请 

















