 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知KspΘ(BaSO4)=1.1×10—10,KspΘ(BaC03)=2.6×10—9,下列说法不正确的是()。A.BaSO4不能转化为
已知KspΘ(BaSO4)=1.1×10—10,KspΘ(BaC03)=2.6×10—9,下列说法不正确的是()。
A.BaSO4不能转化为BaCO3
B.BaCO3可以转化为BaSO4
C.BaSO4可以转化为BaCO3
D.BaSO4与BaCO3可以相互转化
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知KspΘ(BaSO4)=1.1×10—10,KspΘ(BaC03)=2.6×10—9,下列说法不正确的是()。
A.BaSO4不能转化为BaCO3
B.BaCO3可以转化为BaSO4
C.BaSO4可以转化为BaCO3
D.BaSO4与BaCO3可以相互转化
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知KspΘ(BaSO4)=1.1×10—10,KspΘ(B…”相关的问题
更多“已知KspΘ(BaSO4)=1.1×10—10,KspΘ(B…”相关的问题
计算BaSO4在2.0mol/LHCl溶液中的溶解度。已知BaSO4的Ksp=1.1×10-10,H2SO4的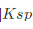 =1.2×10-2。
=1.2×10-2。
将200mL 0.015mol·L-1BaCl2溶液与100mL 0.003mol·L-1Na2SO4溶液混合,判断有无BaSO4沉淀产生。已知Ksp(BaSO4)=1.1×10-10。
A.无沉淀析出
B.有沉淀析出
C.析出沉淀后又溶解
D.不一定
某溶液含有Ba2+、EDTA和


| pH | 8.9 | 9.1 | 9.3 | 9.5 | 9.7 | 10.0 |
| lgY(H) | 1.38 | 1.2 | 1.0 | 0.80 | 0.70 | 0.45 |
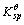 =1.1×10-10。
=1.1×10-10。
向BaCl2溶液中加入过量的Na2SO4溶液,达平衡时()。
A.cr(Ba2+)=cr(SO42—)
B.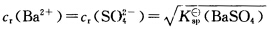
C.cr(Ba2+)<cr(SO42—),<cr(Ba2+).cr(SO42—)=KspΘ(BaSO4)
D.cr(Ba2+)<cr(SO42—),<cr(Ba2+).cr(SO42—)>KspΘ(BaSO4)
某容器内壁覆盖有0.50gCaCO3沉淀,至少需用水多少升才能洗去该沉淀?[已知KspΘ(CaCO3)=8.7×10—9]
Ksp(Ag2CrO4)=1.1×10-12<Ksp(AgCl)=1.8×10-10,在0.1mol·L-1Na2CrO4和0.1mol·L-1NaCl混合液中,逐滴加入AgNO3溶液,先生成沉淀的是______。