 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
自动电位滴定计在滴定开始时,电位测量信号使()断续开、关,滴定自动的进行。
A.控制阀
B.电磁阀
C.乳胶管
D.毛细管
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.控制阀
B.电磁阀
C.乳胶管
D.毛细管
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“自动电位滴定计在滴定开始时,电位测量信号使()断续开、关,滴…”相关的问题
更多“自动电位滴定计在滴定开始时,电位测量信号使()断续开、关,滴…”相关的问题
A.定量分析要求测定结果的误差为零
B.指示剂的酸式色是溶液pH<7时显示的颜色;指示剂的碱式色是溶液pH>7时显示的颜色
C.NaAc的碱性太弱,不能用盐酸直接滴定,可采用回滴的方式测其含量
D.凡氧化剂和还原剂两电对电位之差大于0.4V的氧化还原反应就能用于滴定分析
A.KMnO4电位很高,干扰多,影响反应速率
B.该反应是分步进行的,要完成各步反应需一定时间,但只要反应一形成,速率就快了
C.当第一滴KMnO4与Na2C2O4反应后,产生反应热,加快反应速率
D.反应产生Mn2+,它是KMnO4与Na2C2O4反应的催化剂
E.反应产生CO2,使溶液得到充分搅拌,加快了反应速率
在1mol/L HCl溶液中,用Fe3+滴定Sn2-,计算下列滴定百分数时的电位:9%、50%、91%、99%、99.9%、100%、100.1%、101%、110%、200%。
用K2Cr2O7标准滴定溶液在c(HCl)=1mol/L HCl溶液中滴定Fe2+,反应达化学计量点时的电位是1.02V,求此时Fe3+与Fe2+的浓度比。
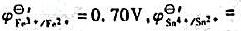 0.14V)
0.14V)
A.采用电位滴定仪检测,没有电位滴定仪的采用 pH 计指示终点
B.使用 pH 计指示终点时,样品温度需调整到 25℃或采用温度补偿功能
C.用电位滴定仪或 pH计,滴定中需要用磁力搅拌器搅拌,滴定至 pH 值 8.30±0.01 并稳定 4-5 秒,整个滴定过程在 1 分钟内完成
D.±0.01 并稳定 4-5 秒,整个滴定过程在 1 分钟内完成
A.避免诱导反应的发生
B.加快反应的速率
C.使指示剂的变色点电位处在滴定体系的电位突跃范围内
D.终点易于观察
E.兼有C与D的作用
在0.1mol·L-1HCl溶液中,用Fe3+滴定Sn2+,其反应为:
2Fe3++Sn2+=2Fe2++Sn4+
(1)计算下列反应的化学计量点的电位和滴定到99.9%和100.1%时的电位。
(2)计算平衡常数及讨论反应进行的完全程度。
在H3PO4存在下的HCl溶液中,用0.1mol/LK2Cr2O7溶液滴定0.1mol/L Fe2+溶液时,已知化学计量点的电位为0.86V。最合适的指示剂为( )。
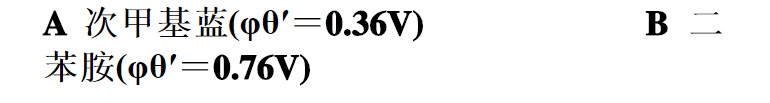
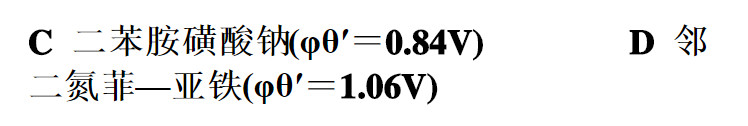
A.0.73V
B.0.89V
C.1.32V
D.1.49V