 更多“将一元弱酸溶液加等体积水稀释时,溶液中H3O+浓度减小到原来…”相关的问题
更多“将一元弱酸溶液加等体积水稀释时,溶液中H3O+浓度减小到原来…”相关的问题
某一弱酸HA的标准解离常数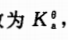 在水溶液中的解离度为α。若加等体积水稀释此洛液,则发生的变化是()。
在水溶液中的解离度为α。若加等体积水稀释此洛液,则发生的变化是()。

A.NaHCO3中含有氢,故其水溶液呈酸性
B.浓HAc(17mol/L)的酸度大于17mol/L H2SO4水溶液的酸度
C.浓度(单位:mol/L)相等的一元酸和一元碱反应后,其溶液呈中性
D.弱酸溶液愈稀,其电离度愈大,因而酸度亦愈大
E.当[H+]大于[OH-]时,溶液呈酸性
A.NaHCO3中含有氧,故其水溶液呈酸性
B.浓HAc(17mol/L)的酸度大于1mol/L H2SO4水溶液的酸度
C.浓度(单位:mol/L)相等的一元酸和一元碱反应后,其溶液呈中性
D.弱酸溶液愈稀,其电离度愈大,因而酸度亦愈大
E.当c(H+)大于c(OH-)时,溶液呈酸性
计算一元弱酸溶液的c(H+),常用的最简式为c(H+)=______,使用此式时要先检查是否满足两个条件:______和______,否则将引入较大误差。
用0.1000mol·L-1NaOH溶液滴定50.00mL一元弱酸的数据如下:
(a)绘制滴定曲线;
(b)绘制 曲线;
曲线;
(c)用二级微商法确定终点;
(d)计算试样中弱酸的浓度;
(e)化学计量点的PH应为多少?
(f)计算此弱酸的电离常数(提示:根据滴定曲线上的半中和点的PH)。
| 体积/mL | pH |
| 0.00 1.00 2.00 4.00 7.00 10.00 12.00 14.00 15.00 15.50 15.60 15.70 15.80 16.00 17.00 20.00 24.00 28.00 | 3.40 4.00 4.50 5.05 5.47 5.85 6.11 6.60 7.04 7.70 8.24 9.43 10.03 10.61 11.30 11.96 12.39 12.57 |
取50.00mL 0.10mol·L-1某一元弱酸溶液,与20mL 0.10mol·L-1NaOH溶液混合后,稀释到100mL。测此溶液的pH=5.25,计算此一元弱酸的Ka。
A.5.3
B.8.7
C.4.3
D.10.7
将2.3182g纯AgNO3配成500.0mL溶液,取出25.00mL溶液置于250mL容量瓶中,稀释至刻度,问所得AgNO3溶液的浓度。


 如果结果不匹配,请
如果结果不匹配,请 



















