 更多“下列氨基酸,在pH=6的缓冲溶液中电泳,移向正极的是()。”相关的问题
更多“下列氨基酸,在pH=6的缓冲溶液中电泳,移向正极的是()。”相关的问题
第1题
在pH=10的氨性缓冲溶液中,用EDTA滴定同浓度的Zn2+到化学计量点时,下列关系哪一种是正确的?() A.c(Zn2+)=
在pH=10的氨性缓冲溶液中,用EDTA滴定同浓度的Zn2+到化学计量点时,下列关系哪一种是正确的?( )

第2题
在下列两种情况下,以EDTA滴定同浓度的Zn2+:一是在pH=10的氨性缓冲溶液中;二是在pH=5.5的六亚甲基四胺缓冲溶液中。滴定前,溶液中Zn2+浓度大小的叙述正确的是( )。
A.两种情况下浓度相等
B.前者大于后者
C.后者大于前者
D.无法判断
E.以上都不正确
第3题
pH=6且含0.001mol/L的Zn2+缓冲溶液50mL,用100mL 0.05mol/L的C9H7NO(8-羟基喹啉)的乙醚溶液萃取,两相分离以
pH=6且含0.001mol/L的Zn2+缓冲溶液50mL,用100mL 0.05mol/L的C9H7NO(8-羟基喹啉)的乙醚溶液萃取,两相分离以后,用原子吸收光谱法测定,已有90%的Zn2+离子被萃取,计算Zn-8羟基喹啉配合物在这个体系中的分配比。
第4题
在下列不同pH的缓冲溶液中,甲基橙的浓度均为2.0x10-4mol·L-1.用1.00cm比色皿,在520cm处测得下列数据:pH 0.88 1.77 2.99 3.41 3.95 4.89 5.50A 0.890 0.890 0.692 0.552 0.385 0.262 0.260试用代数法和图解法求甲基松的pKb值.
第7题
下列关于血浆清蛋白的叙述,不正确的是( )
A.属于球状蛋白质
B.分子量小,在维持血浆胶体渗透压中起主要作用
C.在生理pH条件下,带正电荷
D.在碱性介质中电泳,比所有的球蛋白泳动速度都快
E.饱和硫酸铵可使清蛋白从血浆中沉淀出来
第8题
下列关于缓冲溶液的叙述中,错误的是().
A.缓冲容量越大,则缓冲溶液的缓冲能力越强
B.缓冲比一定时,总浓度越大,缓冲溶液的缓冲能力越强
C.缓冲溶液加水稀释时,缓冲比不变,pH不变,因此缓冲能力也不变
D.HA-A缓冲溶液的缓冲范围为#图片0$#
第9题
当下列电池中的溶液是pH=4.00的缓冲溶液时,在25℃测得电池的电动势为0.209V:玻璃电极当缓冲溶液
当下列电池中的溶液是pH=4.00的缓冲溶液时,在25℃测得电池的电动势为0.209V:玻璃电极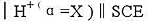 当缓冲溶液由未知溶液代替时,测得电池电动势如下:
当缓冲溶液由未知溶液代替时,测得电池电动势如下:
(a)0.312V; (b)0.088V; (c)-0.017V.试计算每种溶液的pH.
第10题
下列弱酸或弱碱中,最适合于配制pH=9.0缓冲溶液的是( )。
A.羟氨(NH2OH)Kb=1×10-9
B.氨水Kb=1×10-5
C.甲酸Ka=1×10-4
D.乙酸Ka=1×10-5
第11题
已知常温下H3PO4的pKa1=2.16,pKa2=7.21,pKa3=12.32。下列缓冲对中,最适合于配制pH为2.0的缓冲溶液的是()
A.H3PO4-H2PO4-
B.H2PO4--HPO42-
C.HPO42--PO43-
D.H3PO4-PO43-
E.H3PO4-HPO42-


 如果结果不匹配,请
如果结果不匹配,请 


















