 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
实验测得50℃时乙醇(A)-水(B)液态混合物的液相组成xB=0.5561,平衡气相组成yB=0.4289及
气相总压p=24.832kPa,试计算水的活度及活度因子.假设水的摩尔蒸发炜在50~100℃可按常数处理.已知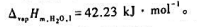
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
气相总压p=24.832kPa,试计算水的活度及活度因子.假设水的摩尔蒸发炜在50~100℃可按常数处理.已知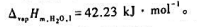
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“实验测得50℃时乙醇(A)-水(B)液态混合物的液相组成xB…”相关的问题
更多“实验测得50℃时乙醇(A)-水(B)液态混合物的液相组成xB…”相关的问题
利用热导检测器分析乙醇、庚烷、苯和乙酸乙酯的混合物。实验测得它们的色谱峰面积分别为5.0cm2、9.0cm2、4.0cm2和7.0cm2。按归一化法,分别计算出它们的质量分数。已知它们的相对质量校正因子fg分别为0.64、0.70、0.78和0.79。
g,测得水:h=4.60cm,W1/2=0.130cm;甲醇:h=4.30cm,W1/2=0.187cm。计算该乙醇的含水量。已知用峰面积表示的相对质量校正因子f水=0.55,f甲醇=0.58;用峰高表示的相对质量校正因子f水=0.224,f甲醇=0.340。
r=1.11x10-9Pa-1,摩尔定压热容Cp,m=114.30J·mol-1·K-1,密度ρ=0.7893g·cm-3.求20℃时液态乙醇的CV,m.
dP(mm) | 3.175 | 6.35 | 9.525 |
R【mol/(s·g(cat))】 | 4.85×10-4 | 4.01×10-4 | 3.54×10-4 |
为了减少固定床反应器的压降,克服粒内阻力,希望采用的最大颗粒直径为多少?
已知
(忽略热效应影响,反应能保证在50℃进行)
A.若进料组成小于95.57%塔不顶可达到98%以上的酒精
B.若进料组成大于95.57%塔釜可达到98%以上的酒精
C.若进料组成小于95.57%塔顶可达到98%以上的酒精
D.若进料组成大于95.57%塔顶不能达到98%以上的酒精
根据实验测得1molH2SO4溶于n1mol水中时,溶解热△isolH可用下式表示
式中a=7.473×104J;b=1.798mol。试求:
实验测得SO2氧化为SO3的反应,在1000K时,各物质的平衡分压为p(SO2)=27.7kPa、p(O2)=40.7kPa、p(SO3)=32.9kPa。计算该温度下反应2SO2(g)+O2(g)====2SO3(g)的平衡常数Kp。