 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
在饱和H2S(Ka9=1.32x10-7,Ka29=7.08x10~15)水溶液中,何者浓度最大()。
A.H2S
B.HS7
C.S2-029
D.H+
E.OH7
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.H2S
B.HS7
C.S2-029
D.H+
E.OH7
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在饱和H2S(Ka9=1.32x10-7,Ka29=7.08…”相关的问题
更多“在饱和H2S(Ka9=1.32x10-7,Ka29=7.08…”相关的问题
在含有0.010mol·dm-3Zn2+、0.10mol·dm-3HAc和0.050mol·dm-3NaAc的溶液中,不断通入H2S使之饱和[c(H2S)=0.10mol·dm-3,问沉淀出ZnS之后溶液中残留的Zn2+浓度是多少?已知HAc: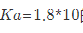
色溶液D。在D中加入饱和H2S溶液生成黑色沉淀E,E可溶于浓硝酸。试判断A,B,C,D,E各为何物?写出相关反应方程式。
下列溶液中能否产生沉淀?(1)0.020mol·L-1BaCl2溶液与0.010mol·L-1Na2CO3溶液等体积混合;(2)0.050mol·L-1MgCl2溶液与0.10mol·L-1氨水等体积混合;(3)在0.10mol·L-1HAc和0.10mol·L-1FeCl2混合溶液中通人H2S气体达饱和(约0.10mol·L-1).
已知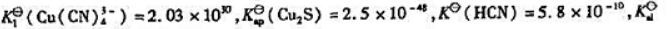
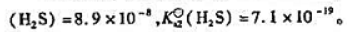
向[Cu(CN)4]3-溶液中通入H2S至饱和,写出反应方程式,计算其标准平衡常数,说明能否生成Cu2S沉淀.
若往含有0.10mol·dm-3ZnCl2和0.10mol·dm-3CuCl2的混合溶液中通入H2S至饱和,按下式计算溶液中Zn2+的浓度:Zn2++H2S====ZnS+2H+。
(已知

H2S:
