 更多“在滴定过程中,由于反应进行的不完全,化学计量点和滴定终点不相…”相关的问题
更多“在滴定过程中,由于反应进行的不完全,化学计量点和滴定终点不相…”相关的问题
第1题
在0.1mol·L-1HCl溶液中,用Fe3+滴定Sn2+,其反应为:2Fe3++Sn2+=2Fe2++Sn4+(1)计算下列反应的化
在0.1mol·L-1HCl溶液中,用Fe3+滴定Sn2+,其反应为:
2Fe3++Sn2+=2Fe2++Sn4+
(1)计算下列反应的化学计量点的电位和滴定到99.9%和100.1%时的电位。
(2)计算平衡常数及讨论反应进行的完全程度。
第4题
(名词配伍)是将化学灭火剂喷入燃烧区参与燃烧反应,中止链反应而使燃烧反应停止。最常见就是用灭火器向着火点喷射灭火。
A. 就是将化学灭火剂喷入燃烧区参与燃烧反应,中止链反应而使燃烧反应停止。最常见就是用灭火器向着火点喷射灭火。
B. 是指可能造成人员伤害,职业病、财产损失、作业环境破坏或这些情况组合的根源或状态。
C. 是管理者对安全生产进行的计划、组织、监督、协调和控制的一系列活动。
D. 是指在生产活动中,由于人们受到科学知识和技术力量的限制,或者由于认识上的局限,而客观存在的可能对系统造成损失的不安全行为或不安全状态。
E. 是指轨道交通机车车辆在运行过程中与行人及其他障碍物相撞,或者轨道交通机车车辆发生脱轨、机车车辆或车站发生火灾、爆炸、拥挤、踩踏、高处坠落、掉下站台、车门等响正常行车。
26. 安全管理()
27. 隐患()
28. 轨道交通事故()
29. 化学抑制灭火法()
30. 危险源()
第5题
用K2Cr2O7标准滴定溶液在c(HCl)=1mol/L HCl溶液中滴定Fe2+,反应达化学计量点时的电位是1.02V,求此时Fe3+与F
用K2Cr2O7标准滴定溶液在c(HCl)=1mol/L HCl溶液中滴定Fe2+,反应达化学计量点时的电位是1.02V,求此时Fe3+与Fe2+的浓度比。
第6题
在25℃,1mol/LHCl溶液中,用Fe3+标准溶液滴定Sn2+液。①计算滴定反应的平衡常数并判断
反应是否完全;②计算化学计量点的电极电位;③计算滴定突跃电位范围,请问可选用哪种氧化还原指示剂指示终点?(已知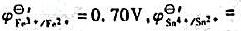 0.14V)
0.14V)
点击查看答案
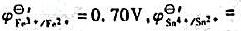 0.14V)
0.14V)
第10题
在滴定反应+6Fe2++14H+→2Cr3++6Fe3++7H2O中,达到化学计量点时,下列各种说法正确的是()。 A.溶液中c(Fe3+)
在滴定反应 +6Fe2++14H+→2Cr3++6Fe3++7H2O中,达到化学计量点时,下列各种说法正确的是( )。
+6Fe2++14H+→2Cr3++6Fe3++7H2O中,达到化学计量点时,下列各种说法正确的是( )。
点击查看答案
 +6Fe2++14H+→2Cr3++6Fe3++7H2O中,达到化学计量点时,下列各种说法正确的是( )。
+6Fe2++14H+→2Cr3++6Fe3++7H2O中,达到化学计量点时,下列各种说法正确的是( )。A.溶液中c(Fe3+)与c(Cr3+)相等
B.溶液中不存在Fe2+和
C.溶液中两个电对Fe3+/Fe2+和
D.溶液中两个电对Fe3+/Fe2+和


 如果结果不匹配,请
如果结果不匹配,请 

















