 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在298K、100kPa下,0.5mol氧气与0.5mol氮气混合,计算此过程的△H、ΔS、ΔG、ΔV。设气体为理想气体。
 答案
答案
此为理想气体的等温等压混合过程,故△H=0,ΔV=0。
ΔG=ΔH-TΔS=-TΔS=1717J
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
此为理想气体的等温等压混合过程,故△H=0,ΔV=0。
ΔG=ΔH-TΔS=-TΔS=1717J
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在298K、100kPa下,0.5mol氧气与0.5mol氮…”相关的问题
更多“在298K、100kPa下,0.5mol氧气与0.5mol氮…”相关的问题
电池Mo(S)|MoS2(S)|H2S(100kPa)|KCl(0.01mol/kg)|HCl(0.01mol/kg)|H2(100kPa)|Pt,测得其在不同温度下的电池电动势数据为 T/K 288 298 308 E/V 0.4148 0.4119 0.4087 (1)写出电极反应和电池反应; (2)由题给数据推导出电池反应的平衡常数与温度的关系式,并计算△rHm; (3)用电化学方法计算298K时电池反应的△rSm,将其与热力学方法计算所得结果相比较可得出什么结论?298K时,物质的规定熵数据为 物质 H(g)H2S(g) Mo(s) MoS2(s) Sm/[J/(K.mol)] 130.6 205.6 28.58 62.59
某种类型的煤含硫为3.0%(质量分数),问: (1)燃烧100g该种煤,将产生多少克二氧化硫? (2)在298K与100kPa下,将产生多少体积的SO2? (3)如采用1.00m3空气燃烧这部分煤,烟道气中SO2的浓度为多少?
计算298K时,Fe3+/Fe2+,c(Fe3+)=0.1mol·L-1, c(Fe2+)=0.5mol·L-1 电对的电极。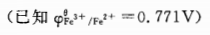
A(g)按下式分解:A(g) 2B(g)。
2B(g)。
(1)在298K时,0.5dm3容器中装有1.588×10-3kg的A(g),平衡时总压力为100kPa。试判断298K,A(g)和B(g)的分压各为150kPa时,上述反应能否自发进行?
(2)若在318K、0.5dm3容器中放入1.35×10-3kg的A(g)时,平衡总压力为105kPa。已知该反应的反应焓与温度的关系为
已知:MA=92.02×10-3kg·mol-1,

已知下列100kPa,298K时的热力学数据:
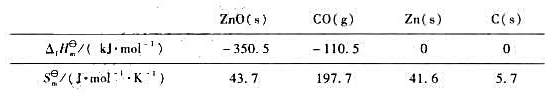
(1)试通过热力学计算,说明下面反应298K时的进行方向:
ZnO(s)+C(s)=Zn(s)+CO(g)
(2)求算上面反应自发正向进行的最低温度。
有5mol He(g),可看做理想气体,已知其CV,m=1.5R,从始态273K、100kPa变到终态298K、1000kPa,求该过程的熵变。
1mol理想气体在298K、101.3kPa下等温可逆膨胀,若过程的△G=-2983J,则终态的压力为多少