 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在一定的条件下,将 2mol SO2和1mol O2充入一定容密闭容器中,发生下列反应:2SO2(g)+O2(g)⇌2SO3(g)△H=-197kJ/mol,当达到平衡状态时,下列说法中正确的是()
A.生成 2 mol SO3
B.放出热量197 kJ
C.SO2 和 SO3 共有 2 mol
D.含有氧原子共有3mol
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.生成 2 mol SO3
B.放出热量197 kJ
C.SO2 和 SO3 共有 2 mol
D.含有氧原子共有3mol
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在一定的条件下,将 2mol SO2和1mol O2充入一定…”相关的问题
更多“在一定的条件下,将 2mol SO2和1mol O2充入一定…”相关的问题
A.①③
B.①④
C.②③
D.③④
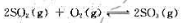
反应达到平衡时,测得混合物中有6.0molSO2(g)。试计算:
(1)该可逆反应在800K时的标准平衡常数和标准摩尔吉布斯自由能变;
(2)SO2在上述条件下的平衡转化率。
已知水在101.325kPa,100℃下的摩尔蒸发焓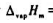 =40.668kJ·mol-1,现有2mol水蒸气在100℃,101.325kPa条件下凝结为液体水,此过程的ΔH=()kJ,Q=()kJ,W=()kJ,ΔU=()kJ.
=40.668kJ·mol-1,现有2mol水蒸气在100℃,101.325kPa条件下凝结为液体水,此过程的ΔH=()kJ,Q=()kJ,W=()kJ,ΔU=()kJ.
用纸色谱法的上行展开法分离


A.决定反应速率的因素只有催化剂
B.食物放在冰箱中会减慢食物变质的速率
C.锌与稀硫酸反应时,加入少量水能加快产生氢气的速率
D.2mol SO2与 1mol O2混合一定能生成2mol SO3
某种类型的煤含硫为3.0%(质量分数),问: (1)燃烧100g该种煤,将产生多少克二氧化硫? (2)在298K与100kPa下,将产生多少体积的SO2? (3)如采用1.00m3空气燃烧这部分煤,烟道气中SO2的浓度为多少?
在375K时反应SO2Cl2(g)=SO2(g)+Cl2(g)的标准平衡常数Kθ为2.4。今将5.4g的SO2Cl2(g)置于密闭容器中,并加热到375K。(1) 假定SO2Cl2(g)不解离,它的压力将是多少?(2) 平衡时SO2Cl2(g)、SO2(g)和Cl2(g)的分压各是多少?