 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
1mol氢,在压强为1.0×105Pa,温度为20℃时,其体积为V0,今使它经以下两种过程达同一状态:
1mol氢,在压强为1.0×105Pa,温度为20℃时,其体积为V0,今使它经以下两种过程达同一状态:(1

 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
1mol氢,在压强为1.0×105Pa,温度为20℃时,其体积为V0,今使它经以下两种过程达同一状态:(1

 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“1mol氢,在压强为1.0×105Pa,温度为20℃时,其体…”相关的问题
更多“1mol氢,在压强为1.0×105Pa,温度为20℃时,其体…”相关的问题
1mol氢,在压强为1.0×105Pa,温度为20℃时,其体积为V0。今使它经以下两种过程达同一状态:(1)先保持体积不变,加热使其温度升高到80℃,然后令它作等温膨胀,体积变为原体积的2倍;(2)先使它作等温膨胀至原体积的2倍,然后保持体积不变,加热到80℃。试分别计算以上两种过程中吸收的热量、气体对外做的功和内能的增量;并作出p-V图。
1mol单原子分子理想气体,在273.2K、1.0×105Pa时发生一变化过程,体积增大一倍,Q=1674J,△H=2092J。
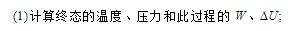

如下图所示,一定量的空气,开始在状态A,其压强为2.0×105Pa,体积为2.0×10-3m3,沿直线AB变化到状态B后,压强变为1.0×105Pa,体积变为3.0×10-3m3,求此过程中气体所做的功。
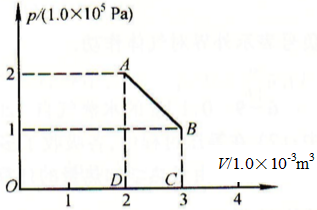
为5×105Pa的氦气,右边充有压强为1×105Pa的氖气,它们都是理想气体.将气缸浸入1l水中,开始时整个物体系的温度均匀地处于25℃.气缸及活塞的热容可不考虑.放松以后振动的活塞最后将位于新的平衡位置,试问这时:
(1)水温升高多少?(2)活塞将静止在距气缸左边多大距离位置?(3)物体系的总熵增加多少?
压强为1.0×105Pa,体积为0.0082m3的氮气,从初始温度300K加热到400K,如加热时(1)体积不变;(2)压强不变,问各需多少热量?哪一过程所需热量大?为什么?
气体的平均自由程可通过实验测定(例如由测量气体的粘度算出气体的平均自由程).现在测得t=20℃,压强为1.0×105Pa时氩和氮的平均自由程分别为

的压强为2.5×103Pa(表压),求管截面上的平均流速。已知当地大气压强为105Pa。
如图所示,管道粗处截面积为A,细处为a,A=16a,设A处压强为2.0×105Pa。

求:
试求压强为1.01×105Pa、质量为2.0g、体积为1.54L的氧气分子的平均平动动能.