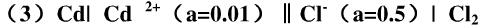题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
有一电池 (-)Pt|H2(50kPa)|H+(0.50mol·L-1)||Sn4+(0.70mol·L-1),Sn2+(0.50mol·L-1)|Pt(+)
有一电池(-)Pt,H2(50kPa)|H+(0.50mol·L-1)||Sn4+(0.70mol·L-1),Sn2+(0.50mol·L-1)|Pt()
(1)写出半反应
(2)写出电池反应
(3)计算原电池的电动势E
(4)当E=0时,在保持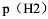 和
和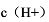 不变的情况下,
不变的情况下,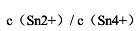 等于多少?
等于多少?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“有一电池 (-)Pt|H2(50kPa)|H+(0.50mo…”相关的问题
更多“有一电池 (-)Pt|H2(50kPa)|H+(0.50mo…”相关的问题
![在电池Pt|H2(g,100kPa)|HI溶液[ɑ(HI)=1]|I2(s)|Pt中,进行如下两个电](https://img2.soutiyun.com/ask/2020-11-23/974976417829079.png)
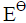 =0.2680V:
=0.2680V: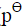 )|HCl(0.08mol·kg-1, γ±=0.809)|Hg2Cl2(s)|Hg(l)
)|HCl(0.08mol·kg-1, γ±=0.809)|Hg2Cl2(s)|Hg(l)
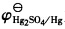 为0.6158V。
为0.6158V。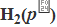 |Pt
|Pt


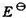 =0.9265V;
=0.9265V;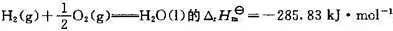 ;
;