 更多“在一定温度下反应的活化能越大,反应速率也越大。()”相关的问题
更多“在一定温度下反应的活化能越大,反应速率也越大。()”相关的问题
A.反应级数愈大,反应速度,活化能越大,反应速度越快
B.一般化学反应应在一定的温度范围内,温度每升高10K反应速度约增加2~4倍
C.反应速度只决定于速度,温度相同时各反应速度常数相等
D.活化能越大,反应速度越快在A+BC反应中,若增加压强或者降低温度,B的转化率增大,则反应体系中
某二级反应,其在不同温度下的反应速率常数如下:
T/K 645 675 715 750
k×103/(mol-1·L·min-1) 6.15 22.0 77.5 250
(1)作lnk-1/T图,计算反应活化能Ea;
(2)计算700K时的反应速率常数k。
半水合磷酸铡晶体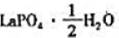 受热时将失去结晶水,而得到无水磷酸镧
受热时将失去结晶水,而得到无水磷酸镧
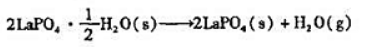
在不同温度下该反应速率常数如表3—4.

用不同的方法计算该反应的活化能.
A.高温下分子碰撞更加频繁
B.反应物分子所产生的压力随温度升高而增大
C.反应的活化能随温度的升高而减小
D.活化分子的百分率随温度升高而增大
一般反应温度上升10℃,反应速率增大一倍(即为原来的2倍)。为了使这一规律成立,活化能与温度间应保持怎样的关系?并求出下列温度下的活化能。
温度(K):300,400,600,800,1000。
氨合成塔入口的气体组成(摩尔分数)为NH33.5%,N220.87%,H262.6%,Ar7.08%及CH45.89%。该塔在30MPa压力下操作。已知催化剂床层中某处的温度为490℃,反应气体中氨含量为10%(摩尔分数)。试计算该处的反应速率。在Fe催化剂上氨合成反应速率式为
逆反应的活化能
。450℃时,k2=1.02×105kmol·Pa0.5/(m3·h),且
;490℃时,Kp可按下式计算:
已知反应2H2O2====2H2O+O2的活化能Ea为71kJ·mol-1,在过氧化氢酶的催化下,活化能降至8.4kJ·mol-1。试计算298K时在酶催化下,H2O2分解速率为原来的多少倍?


 如果结果不匹配,请
如果结果不匹配,请 

















