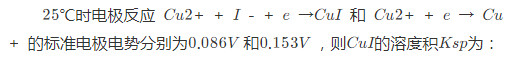更多“求下列电极在298.15K时的电极电势。”相关的问题
更多“求下列电极在298.15K时的电极电势。”相关的问题
已知298.15K时,电极反应: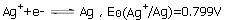 ,Ag2C2O4的Ksp为3.5×10-11,求电极反应Ag2C2O2+2e-
,Ag2C2O4的Ksp为3.5×10-11,求电极反应Ag2C2O2+2e- 2Ag+C2O2-4的标准电极电势
2Ag+C2O2-4的标准电极电势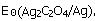 。
。
已知298.15K时, ,
, ,标准态时:(1)写出原电池符号(应自发进行);(2)写出电极反应及电池反应;(3)计算原电池的
,标准态时:(1)写出原电池符号(应自发进行);(2)写出电极反应及电池反应;(3)计算原电池的 ;(4)计算电池反应的
;(4)计算电池反应的 ;(5)求AgI的Ksp。
;(5)求AgI的Ksp。
已知25℃时,电极OH-|Ag2O(s)|Ag及OH-,H2O|O2的标准电极电势分别为0.344V,△H=0.401V;-31.05kJ·mol-1,且其值不随温度而改变;空气的压力为101.325kPa,其中O2的摩尔分数为0.21。试求Ag2O(s)在空气中的分解温度为若干?
A.
B.同一元素有多种氧化态时,不同氧化态组成的电对的
C.电对中有气态物质时,
D.由同一金属不同氧化态的离子组的氧化还原电极,当氧化态和还原态浓度相等时的电极电势就是标准电极电势
298.15K时,柠檬酸(H3Cit)的


查表写出下列电极反应的标准电极电势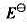 据此回答下列问题:
据此回答下列问题:
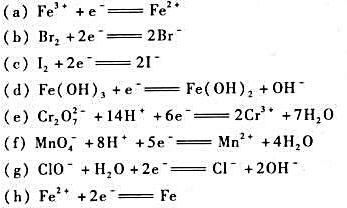
(1)哪些电极反应的电极电势值不受介质的酸碱性影响?
(2)哪种物质是酸性介质中最强的氧化剂?哪种物质是碱性介质中最强的还原剂?
(3)在标准状态下,哪些物质可以将Br-氧化?
(4)在标准状态下,哪些物质可以将Fe3+还原?
(5)降低pH,哪些电极反应的电极电势值升高?
电极反应: ,计算电对
,计算电对



根据298.15K,pΘ时物质的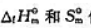 值,(1)求下列反应CO2(g)+2NH3(g)=CO(NH2)2(s)+H2O(l)的
值,(1)求下列反应CO2(g)+2NH3(g)=CO(NH2)2(s)+H2O(l)的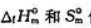 ;(2)计算上述反应在298.15K及pΘ下的ΔrGΘm值,.并判断由CO2(g)和NH3(g)反应生成尿素是否为自发过程.
;(2)计算上述反应在298.15K及pΘ下的ΔrGΘm值,.并判断由CO2(g)和NH3(g)反应生成尿素是否为自发过程.

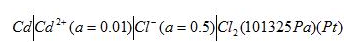

 如果结果不匹配,请
如果结果不匹配,请