 更多“分别计算下列各混合溶液中的pH;”相关的问题
更多“分别计算下列各混合溶液中的pH;”相关的问题
第1题
25℃时,pH(HAc)=4.74。将20mL0.10mol·L-1HAc溶液与10ml.0.10mol·L-1NaOH溶液混合.计算所得混合溶液的pH。
25℃时,pH(HAc)=4.74。将20mL0.10mol·L-1HAc溶液与10ml.0.10mol·L-1NaOH溶液混合.计算所得混合溶液的pH。
点击查看答案
第2题
25℃时二元弱酸H2B的试计算: (1)25℃时0.10mol·L-1H2B溶液的pH; (2)25℃时0.10
25℃时二元弱酸H2B的试计算: (1)25℃时0.10mol·L-1H2B溶液的pH; (2)25℃时0.10
点击查看答案
25℃时二元弱酸H2B的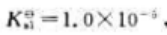
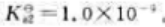
试计算:
(1)25℃时0.10mol·L-1H2B溶液的pH;
(2)25℃时0.10mol·L-1NaHB溶液的pH;
(3)25℃时0.10mol·L-1.H2B0.010mol·L-1NaHB混合溶液的pH:
(4)25℃时0.10mol·L-1Na2B溶液的pH。
第3题
在Bi3+和Ni2+均为0.02mol/L时的混合溶液中,试求以EDTA溶液滴定时所允许的最小pH。能否采用控制溶液酸度的方
在Bi3+和Ni2+均为0.02mol/L时的混合溶液中,试求以EDTA溶液滴定时所允许的最小pH。能否采用控制溶液酸度的方法实现二者的分别滴定?
第4题
今有0.10mol.L-1 Na2B4O7。溶液500mL,(1) 求溶液的pH(不考虑离子强度的影响
今有0.10mol.L-1Na2B4O7。溶液500mL,(1) 求溶液的pH(不考虑离子强度的影响
点击查看答案
今有0.10mol.L-1Na2B4O7。溶液500mL,(1) 求溶液的pH(不考虑离子强度的影响):欲用上述溶液分别配制(2)pH=9.00,(3)pH=10.00的缓冲溶液。问各应加入什么溶液?各应加入多少毫升(设其浓度为2.0mol.L-1)?已知H3BO3的pK=9.24。
第6题
下列各混合溶液,哪些具有对溶液pH的缓冲能力?( )
A.100mL 1mol/L HAc+100mL 1mol/L NaOH
B.100mL 1mol/L HCl+200mL 2mol/L NH3·H2O
C.200mL 1mol/L HAc+100mL 2mol/L NaOH
D.100mL 1mol/L NH4Cl+100mL 1mol/L NH3·H2O
E.100mL 5mol/L NaOH+100mL 0.1mol/L HCl
第7题
0.35mol·L-1 HAc溶液与0.45mol·L-1NaAc 等体积混合,计算混合溶液的pH值。
0.35mol·L-1 HAc溶液与0.45mol·L-1NaAc 等体积混合,计算混合溶液的pH值。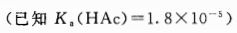
第9题
有一Zn2+、Mg2+混合溶液,通过计算说明在pH=5.0时可否滴定Zn2+而Mg2+不干扰?
有一Zn2+、Mg2+混合溶液,通过计算说明在pH=5.0时可否滴定Zn2+而Mg2+不干扰?
第10题
称取0.5000g白云石样品,溶于酸后定容成250mL,吸取25.00mL,加掩蔽剂消除干扰,在pH=10时用K~B混合指示剂,以0.
02000mol·L-1EDTA滴定,用去26.26mL。又另吸25.00mL溶液,加掩蔽剂后,在pH=12.5时以钙指示剂指示终点,用同浓度的EDTA滴定,用去13.12mL,计算试样中CaCO3和MgCO3的含量。
点击查看答案
第11题
取50.00mL 0.10mol·L-1某一元弱酸溶液,与20mL 0.10mol·L-1NaOH溶液混合后,稀释到100mL。测此溶液的pH=5.25,
取50.00mL 0.10mol·L-1某一元弱酸溶液,与20mL 0.10mol·L-1NaOH溶液混合后,稀释到100mL。测此溶液的pH=5.25,计算此一元弱酸的Ka。


 如果结果不匹配,请
如果结果不匹配,请 


















