 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
在一密闭容器中盛有过量的NaHCO3和少量的Na2O2,将其加热到300℃经充分反应后,排出气体,容器内残留的固体是()。
A.NaHCO3和NaOH
B.Na2CO3和NaOH
C.NaHCO3和Na2CO3
D.只有Na2CO3
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.NaHCO3和NaOH
B.Na2CO3和NaOH
C.NaHCO3和Na2CO3
D.只有Na2CO3
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在一密闭容器中盛有过量的NaHCO3和少量的Na2O2,将其…”相关的问题
更多“在一密闭容器中盛有过量的NaHCO3和少量的Na2O2,将其…”相关的问题
g)和H2O(l)。过程放热401.727kJ。求
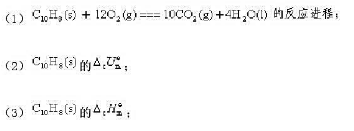
在一密闭容器中,储有A、B、C三种理想气体,处于平衡状态.A种气体的分子数密度为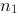 ,它产生的压强为
,它产生的压强为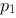 ,B种气体的分子数密度为
,B种气体的分子数密度为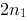 ,C种气体的分子数密度为
,C种气体的分子数密度为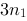 ,则混合气体的压强 p为
,则混合气体的压强 p为
A、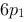
B、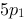
C、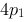
D、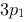
在一定温度下,将1.0molNa2O2(g)放入一密闭容器中,发生下列可逆反应
 当达到化学平衡时,容器内有0.8molNO,气体总压为100kPa。则该可逆反应在此温度下的标准平衡常数为().
当达到化学平衡时,容器内有0.8molNO,气体总压为100kPa。则该可逆反应在此温度下的标准平衡常数为().
A、0.40
B、0.67
C、0.76
D、1.3
设有一反应2A(g)+B(g)→G(g)+H(s)在某恒温密闭容器中进行,开始时A和B的物质的量之比为2:1,起始总压为3.0kPa,在400K时,60s后容器中的总压力为2.0kPa,设该反应的速率方程为
在一密闭容器中进行反应 ,SO2的起始浓度是0.4mol·L-1,O2的起始浓度是1mol·L-1,当80%的SO2转化为SO3时反应达到平衡,计算平衡时的三种气体的浓度和平衡常数。
,SO2的起始浓度是0.4mol·L-1,O2的起始浓度是1mol·L-1,当80%的SO2转化为SO3时反应达到平衡,计算平衡时的三种气体的浓度和平衡常数。
