 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在温度为298K、100kPa压力下,已知C(金刚石)和C(石墨)的摩尔熵、摩尔燃烧焓和密度分别为(1)在298
在温度为298K、100kPa压力下,已知C(金刚石)和C(石墨)的摩尔熵、摩尔燃烧焓和密度分别为
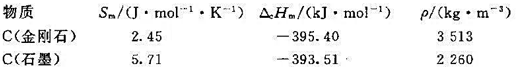
(1)在298 K及100 kPa下,试求C(石墨)→C(金刚石)的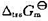 ;
;
(2)在298K及100kPa下,哪个晶体更为稳定?
(3)增加压力能否使不稳定的晶体向稳定晶体转化?如有可能,至少要加多大的压力,才能实现这种转化?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“在温度为298K、100kPa压力下,已知C(金刚石)和C(…”相关的问题
更多“在温度为298K、100kPa压力下,已知C(金刚石)和C(…”相关的问题

 2B(g)。
2B(g)。 ,求a、b的值。
,求a、b的值。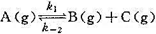 ,已知在298 K时,k1=0.21s-1,k-2=5×10-9Pa-1·s-1,当温度由298 K升到310 K时,k和k-2的值均增加1倍,试求:
,已知在298 K时,k1=0.21s-1,k-2=5×10-9Pa-1·s-1,当温度由298 K升到310 K时,k和k-2的值均增加1倍,试求: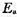 ;
;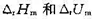 ;
;
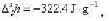 过冷水和冰的饱和蒸气压分别为
过冷水和冰的饱和蒸气压分别为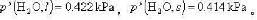 今在100kPa下,有-5°C1kg的过冷水变为同样温度、压力下的冰,设计可逆途径,分别按可逆途径计算过程的ΔS及ΔG.
今在100kPa下,有-5°C1kg的过冷水变为同样温度、压力下的冰,设计可逆途径,分别按可逆途径计算过程的ΔS及ΔG.
















