 更多“在电位滴定中,绘制微商滴定曲线可提高对滴定终点判断的准确度(…”相关的问题
更多“在电位滴定中,绘制微商滴定曲线可提高对滴定终点判断的准确度(…”相关的问题
第3题
电位滴定中,以作图绘制滴定曲线( ),( )和( )分别对应的是化学计量点的体积。
电位滴定中,以作图绘制滴定曲线(),()和()分别对应的是化学计量点的体积。
点击查看答案
电位滴定中,以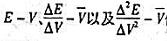 作图绘制滴定曲线(),()和()分别对应的是化学计量点的体积。
作图绘制滴定曲线(),()和()分别对应的是化学计量点的体积。
第4题
一自动电势滴定仪以0.1mL·S-1的恒定速度滴加滴定剂.按设计要求,当二次微商滴定曲线为零
时,仪器自动关闭滴液设置,但由于机械延迟,关闭时间晚了2s.如果用这台滴定仪以0.10mol·L-1的Ce4+来滴定50mL0.1mol·L-1的Fe2+,由于延迟将引起多大的误差?当滴定仪关闭时,电势将是多少?
点击查看答案
[已知φθ(Ce4+/Ce3+)=1.28V]
第5题
用0.1000mol·L-1NaOH溶液滴定50.00mL一元弱酸的数据如下: 体积/mL pH 0.001.002.004.007.0
用0.1000mol·L-1NaOH溶液滴定50.00mL一元弱酸的数据如下:
(a)绘制滴定曲线;
(b)绘制 曲线;
曲线;
(c)用二级微商法确定终点;
(d)计算试样中弱酸的浓度;
(e)化学计量点的PH应为多少?
(f)计算此弱酸的电离常数(提示:根据滴定曲线上的半中和点的PH)。
| 体积/mL | pH |
| 0.00 1.00 2.00 4.00 7.00 10.00 12.00 14.00 15.00 15.50 15.60 15.70 15.80 16.00 17.00 20.00 24.00 28.00 | 3.40 4.00 4.50 5.05 5.47 5.85 6.11 6.60 7.04 7.70 8.24 9.43 10.03 10.61 11.30 11.96 12.39 12.57 |
第6题
用Fe3+滴定Sn2+时,下列有关滴定曲线的叙述中,不正确的是 ()A.滴定百分率为100%处的电位为
用Fe3+滴定Sn2+时,下列有关滴定曲线的叙述中,不正确的是 ()
A.滴定百分率为100%处的电位为计量点电位
B.滴定百分率为50%处的电位为Sn4+/Sn2+电对的条件电位
C.滴定百分率为200%处的电位为Fe3+/Fe2+电对的条件电位
D.滴定百分率为25%处的电位为Sn4+/Sn2+电对的条件电位
第9题
在25℃,1mol/LHCl溶液中,用Fe3+标准溶液滴定Sn2+液。①计算滴定反应的平衡常数并判断
反应是否完全;②计算化学计量点的电极电位;③计算滴定突跃电位范围,请问可选用哪种氧化还原指示剂指示终点?(已知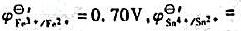 0.14V)
0.14V)
点击查看答案
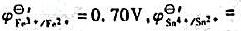 0.14V)
0.14V)
第10题
以下说法除()以外都是错误的。
A.定量分析要求测定结果的误差为零
B.指示剂的酸式色是溶液pH<7时显示的颜色;指示剂的碱式色是溶液pH>7时显示的颜色
C.NaAc的碱性太弱,不能用盐酸直接滴定,可采用回滴的方式测其含量
D.凡氧化剂和还原剂两电对电位之差大于0.4V的氧化还原反应就能用于滴定分析


 如果结果不匹配,请
如果结果不匹配,请 



















